

Sarcoidosis como causa de fiebre de origen desconocido: presentación de caso
Sarcoidosis as a Cause of Fever of Unknown Origin: Case Report
Sarcoidose como causa de febre de origem desconhecida: relato de caso
Sarcoidosis como causa de fiebre de origen desconocido: presentación de caso
Revista Ciencias de la Salud, vol. 20, núm. 2, 2022
Universidad del Rosario
Recibido: 26 enero 2022
Aceptado: 30 marzo 2022
Información adicional
Para citar este artículo: Arango Rivas AM, Castilla Agudelo GA, Chavarriaga Restrepo A, Velásquez Franco CJ, Varela Aguirre GJ. Sarcoidosis como causa de fiebre de origen desconocido: presentación de caso. Rev Cienc Salud. 2022;20(2):1-9. https://doi.org/10.12804/revistas.urosario.edu.co/revsalud/a.10371
Resumen: Introducción: en el enfoque de los pacientes con fiebre de origen desconocido es importante tener en cuenta las etiologías inflamatorias no infecciosas, entre ellas enfermedades del tejido conectivo, vasculitis y granulomatosas. La sarcoidosis es inflamatoria, idiopática, crónica, multisistémica, granulomatosa y es una causa de fiebre de origen desconocido. Presentación del caso: se presenta el caso de un paciente con fiebre y manifestaciones cutáneas sugestivas de endocarditis y lesiones nodulares dolorosas en la región pretibial. Se descartó esta etiología por ecocardiografía transesofágica, con hemocultivos negativos y sin claro foco infeccioso ni respuesta a antibióticos de amplio espectro. Se le realizó una tomografía por emisión de positrones con evidencia de adenopatías en ambos hilios pulmonares y una biopsia de piel que evidenció granulomas sin necrosis, sin vasculitis, paniculitis con infiltrado septal. Conclusiones: por un cuadro clínico sugestivo y hallazgos radiológicos, se sospechó de sarcoidosis y se inició su manejo con posterior resolución del cuadro.
Palabras clave: sarcoidosis, sarcoidosis pulmonar, paniculitis, fiebre de origen desconocido, enfermedad granulomatosa.
Abstract: Introduction: In the approach to patients with fever of unknown origin, it is important to take into account non-infectious inflammatory diseases, including connective tissue diseases, vasculitis and granulomatous diseases. Sarcoidosis is an idiopathic, chronic, multisystemic, granulomatous inflammatory disease and is a cause of fever of unknown origin. Case presentation: There is the case of a patient with fever and skin manifestations suggestive of endocarditis and painful nodular lesions in the pretibial region. This etiology was ruled out by transesophageal echocardiography, with negative blood cultures and without a clear infectious focus or response to broad-spectrum antibiotics. pet/ct was performed with evidence of lymphadenopathy in both pulmonary hila and skin biopsy evidence of granulomas without necrosis, without vasculitis, with septal infiltrate. Conclusions: By suggestive clinical picture and radiological findings, sarcoidosis is suspected and management is started with subsequent resolution of its picture.
Keywords: Sarcoidosis, pulmonary sarcoidosis, panniculitis, unknown origin fever, granulomatous disease.
Resumo: Introdução: na abordagem de pacientes com febre de origem desconhecida, é importante levar em consideração etiologias inflamatórias não infecciosas, incluindo doenças do tecido conjuntivo, vasculites e doenças granulomatosas. A sarcoidose é uma inflamação idiopática, crônica, multissistêmica, granulomatosa e causa febre de origem desconhecida. Apresentação do caso: apresentamos o caso de um paciente com febre e manifestações cutâneas sugestivas de endocardite e lesões nodulares dolorosas na região pré-tibial. Essa etiologia foi descartada pelo ecocardiograma transesofágico, com hemoculturas negativas e sem foco claro de infecção ou resposta a antibióticos de amplo espectro. Foi realizada tomografia por emissão de pósitrons com evidência de linfadenopatias em ambos os hilos pulmonares e na biópsia de pele evidência de granulomas sem necrose, sem vasculite, paniculite com infiltrado septal. Conclusões: devido ao quadro clínico sugestivo e aos achados radiológicos, suspeita-se de sarcoidose e inicia-se o manejo com posterior resolução do quadro.
Palavras-chave: sarcoidose, sarcoidose pulmonar, paniculite, febre de origem desconhecida, doença granulomatosa.
Introducción
La fiebre de origen desconocido (fod) sigue siendo un reto clínico a pesar de los avances en las técnicas de diagnóstico. Las causas de la fod se clasifican en infecciosas, neoplásicas, inflamatorias no infecciosas y otras causas, como la fiebre inducida por medicamentos y la fiebre facticia (1). Las etiologías inflamatorias no infecciosas comprenden las enfermedades del tejido conectivo, vasculitis y enfermedades granulomatosas (2). En este último grupo se encuentra la sarcoidosis, cuya etiología es desconocida, crónica, multisistémica y con evidencia histológica de granulomas no caseificantes (3). La prevalencia estimada es de 10 a 20 por cada 100000 habitantes, y es más común entre los afroamericanos que entre los blancos (4). Su diagnóstico se basa en la exclusión de otras causas que puedan causar granulomas con necrosis sin caseificación, sumado al compromiso de, al menos, dos órganos, en un paciente con síntomas compatibles (5). Es más común en mujeres y más grave en afroamericanos, y se ha observado principalmente en jóvenes adultos entre 20 y 40 años, con un segundo pico en la sexta década (6,7). Más del 90% de los casos muestran afectación pulmonar, por lo que la obtención de imágenes torácicas es clave para el diagnóstico (8). Es por esto por lo que la sarcoidosis es considerada por muchos un reto diagnóstico, no solo por la complejidad de sus manifestaciones, sino también por la similitud con otras condiciones multisistémicas, como infecciones y enfermedades autoinmunes, las cuales deben excluirse en el abordaje del paciente con fod.
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes. Los autores han obtenido el consentimiento informado del paciente referido en el artículo. Este documento obra en poder del autor de correspondencia.
Presentación de caso
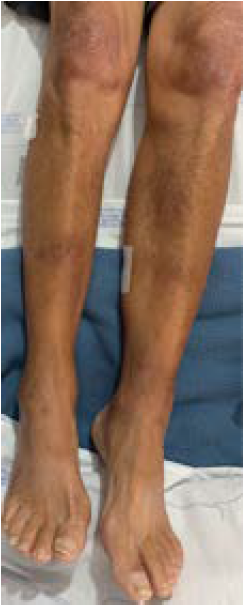
El caso corresponde a un hombre de 66 años de edad, mestizo, residente en Medellín (Colombia), quien trabajó con textiles. Era independiente para todas sus actividades y consultó de forma extrainstitucional por un cuadro clínico de 15 días de evolución, consistente en la aparición de lesiones eritematosas y dolorosas en las palmas de las manos asociadas con edema, el cual se autolimitó. Posteriormente, las mismas lesiones aparecieron en la región pretibial, con fiebre, y asociadas con un dolor intenso, así como en los tobillos. No había pérdida de peso, fiebre, síntomas respiratorios o gastrointestinales. Tenía una pobre evolución, con persistencia de la fiebre y aumento del dolor.
En el examen físico su presión arterial fue de 135/70 mmHg; la frecuencia cardiaca, de 100 lpm; la temperatura axilar, de 38,3°C, con petequias subconjuntivales en ambos ojos, hemorragias en astilla, placas eritematosas y nódulos en las palmas (figura 1) y región pretibial, clínicamente sospechosas de paniculitis.
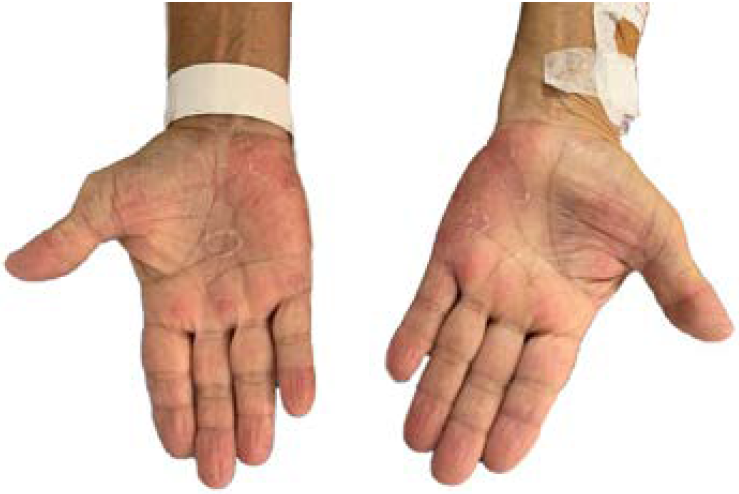
Se sospechó de endocarditis infecciosa por clínica y se le solicitaron exámenes paraclínicos iniciales (tabla 1). No se le realizó la prueba de enzima convertidora de angiotensina (eca), porque no estaba disponible en la institución. Se le tomaron hemocultivos y se inició un manejo antibiótico con 2 gramos de ceftriaxona cada 24 horas y con un gramo de vancomicina cada 12 horas, y ecocardiografía transtorácica.
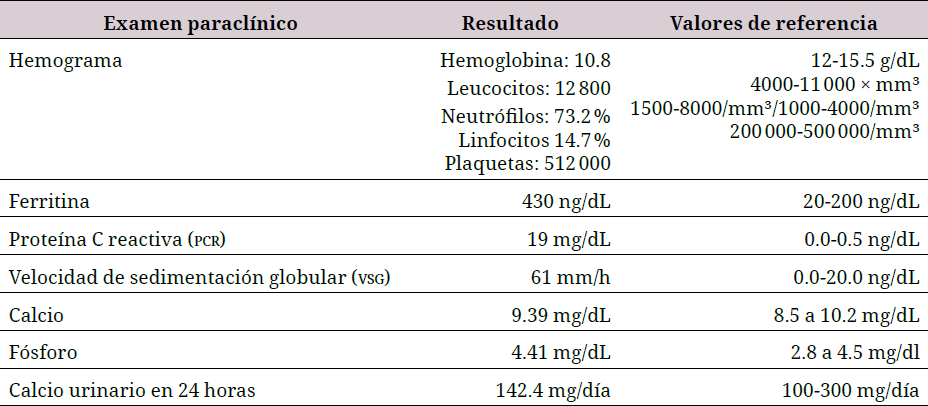
Fueron normales la función hepática, todo el perfil infeccioso y autoinmune, al igual que el calcio sérico y la calciuria de 24 horas.
Se le tomó una ecocardiografía transtorácica sin encontrar vegetaciones ni hallazgos sugestivos de endocarditis; adicionalmente, los hemocultivos fueron negativos. Al principio, el paciente tuvo una buena respuesta al manejo antibiótico; sin embargo, tuvo un nuevo pico febril de 39°C, por lo que se le solicitó una ecocardiografía transesofágica, con la que se descartó nuevamente la endocarditis.
El paciente cumplía criterios de fod; por ello, se le solicitó una tomografía axial computarizada (tac) de abdomen contrastado, cuyo resultado fue normal, y una tac contrastada de tórax, con evidencia de adenopatías en ambos hilios pulmonares y en ambas axilas, junto con derrame pleural, que no se estudió. Adicionalmente, se le practicaron una endoscopia y una colonoscopia, que no mostraron alteraciones. En el entretanto, el hombre mantenía los picos febriles y aumentaban los nódulos dolorosos en la región pretibial. Se suspendieron los antibióticos y se remitió a un hospital de tercer nivel de complejidad.
El paciente ingresó estable hemodinámicamente con dolor en las lesiones nodulares de la región pretibial y artralgias desproporcionadas en sus tobillos, sin sinovitis. Se le tomó una tomografía por emisión de positrones, que evidenció un aumento del metabolismo en la piel, en el tejido celular subcutáneo, en el cuero cabelludo y en las extremidades, con mayor metabolismo en manos, rodillas, piernas, tobillos y pies (figura 2). En el pulmón había mayor actividad en el ápice del lóbulo superior derecho, con adenopatías en ambos hilios pulmonares y axilares, pero sin evidencia de alguna patología tumoral o cardiaca.
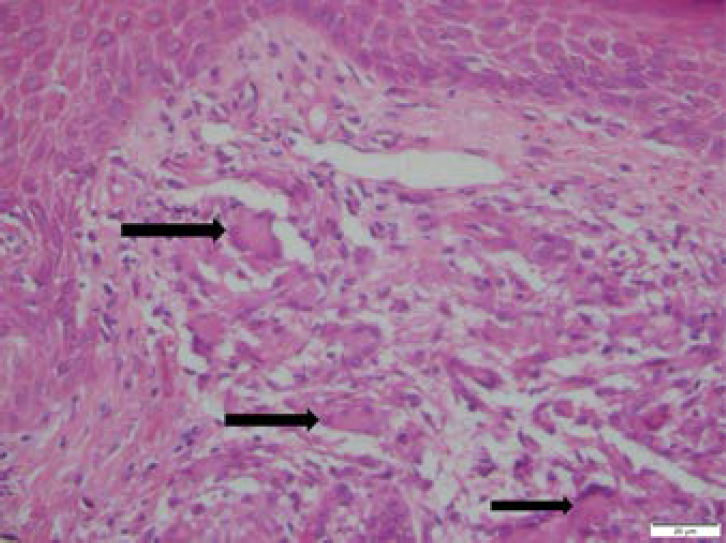
Por lo anterior, se le practicó al paciente un lavado brancoalveolar, a partir del cual y mediante la proteína C reactiva, no se aislaron bacterias, micobacterias u hongos, para Mycobacterium tuberculosis. Se decidió, entonces, realizarle una biopsia de sus nódulos palmares, en lugar de las adenopatías hiliares, por el riesgo de complicaciones asociadas con esta. Según la biopsia palmar, había múltiples granulomas epitelioides sin necrosis central, localizados en la dermis papilar y reticular sin vasculitis. En la biopsia pretibial había infiltrado septal, con presencia de granuloma sin necrosis y sin vasculitis (figura 3). Por el cuadro clínico sugestivo y por los hallazgos imagenológicos, se sospechó de sarcoidosis y se inició el manejo con 20 miligramos semanales vía oral de metotrexate y con 30 miligramos de prednisona diarios. A partir de ahí hubo una mejoría clínica significativa, sin nuevos episodios febriles y con resolución de las lesiones en la piel en menos de una semana.
Discusión
Tres categorías generales de etiologías representan la mayoría de los casos de fod “clásicos”. Estas incluyen infecciones, neoplasias y causas reumatológicas sistémicas.
En el contexto de lo descrito, ante un paciente con fod, deben sospecharse y descartarse las condiciones inflamatorias no infecciosas, basándose en el criterio clínico y en la probabilidad pretest de una enfermedad autoinmune, la cual surge de un minucioso diagnóstico diferencial que excluye causas infecciosas, neoplásicas y sistémicas no autoinmunes (1).
En el momento de abordar a un paciente con sospecha de sarcoidosis se debe realizar una evaluación integral, que incluya antecedentes, examen físico, radiografía del tórax, pruebas de función pulmonar, hemograma, examen de orina, electrocardiograma, examen oftalmológico y prueba de tuberculina. Todo esto para respaldar el diagnóstico de sarcoidosis y evaluar su gravedad y extensión, además de descartar diagnósticos alternativos (9).
El diagnóstico requiere manifestaciones clínicas y radiográficas compatibles, exclusión de otras causas que puedan presentarse de manera similar y detección histopatológica de granulomas no caseificantes. En una serie de casos del nororiente colombiano, donde se incluyeron a ocho pacientes con sarcoidosis, el síntoma más frecuente fue disnea (75%), seguido por tos, pérdida de peso y dolor torácico en el 50% de los casos (10). La fiebre estuvo presente en tres pacientes (37.8%). La afectación pulmonar se observó en un 50% de los individuos, y fue característico el compromiso bilateral y de los lóbulos superiores.
Por otro lado, en una serie de 22 pacientes de Medellín (Colombia), reportada por Muñoz et al., se encontró como principal causa de consulta los síntomas cutáneos y articulares (11). Catorce pacientes tenían síntomas pulmonares y hallazgos cutáneos determinados por eritema nodoso, pápulas, cambios en tatuaje y síndrome de Sweet. En el 62% de los casos se reportaron síntomas articulares y cuatro sujetos (18.1%) tenían pérdida de peso y fiebre. Por lo anterior, la fiebre no es uno de los principales síntomas predominantemente descritos en pacientes con sarcoidosis; sin embargo, puede ser un motivo de hospitalización. Además, la serie colombiana más grande de sarcoidosis no documentó la fiebre como la manifestación inicial (12).
Si bien este no fue el caso, es fundamental considerar que los pacientes que presentan adenopatía hiliar bilateral asintomática o un síndrome de Löfgren clásico (fiebre, eritema nudoso, artralgias y linfadenopatía hiliar bilateral), síndrome de Heerfordt con fiebre uveoparotídea o lupus pernio no requieren biopsia si las anomalías se resuelven rápida y espontáneamente (9). Las imágenes pulmonares cumplen un papel esencial en el diagnóstico de sarcoidosis, tanto la radiografía de tórax como la tac. Otras pruebas por imágenes, como la tomografía por emisión de positrones con flúor-18-fluorodesoxiglucosa (fdg-pet), a veces, son útiles para identificar lesiones ocultas que son más accesibles a la biopsia, así como en la evaluación de la sarcoidosis cardiaca (13,14). En este caso, la importancia de la fdg-pet fue describir un compromiso por adenopatías en ambos hilios pulmonares, además de descartar la afectación cardiaca y tumoral.
En nuestro paciente, por el cuadro clínico sugestivo y los hallazgos imagenológicos, se sospechó sarcoidosis. La biopsia de las lesiones nodulares en la región palmar confirmó los granulomas epitelioides sin necrosis central y sin vasculitis; entre tanto, la biopsia pretibial, el infiltrado septal, con presencia granuloma sin necrosis sin vasculitis. Por lo anterior, se inició el manejo con 20 miligramos vía oral semanales de metotrexate y de 30 miligramos diarios de prednisona. Con ello, el paciente tuvo una mejoría clínica significativa, sin nuevos episodios febriles y con resolución de las lesiones en la piel en menos de una semana.
Finalmente, el diagnóstico de sarcoidosis se basa en un cuadro clínico e imagenológico compatible, así como en signos histológicos y la exclusión de etiologías que puedan tener una presentación similar. Varios informes han demostrado el valor de la pet para detectar la enfermedad oculta que puede, además, ayudar a determinar un sitio para la biopsia. Por ser esta una entidad difícil de diagnosticar, es importante tenerla en cuenta entre los diagnósticos diferenciales de los pacientes con fod, con afectación cutánea y pulmonar, en quienes se descartaron causas infecciosas, neoplásicas y sistémicas tanto autoinmunes y no autoinmunes.
Contribución de los autores
Todos los autores contribuyeron a la adquisición de los datos e información, revisión de contenido intelectual importante y aprobación final de la versión por ser publicada.
Financiación
Recursos propios. El trabajo no fue respaldado por alguna beca o por fondos de la industria farmacéutica.
Conflictos de intereses
Ninguno declarado.
Referencias
1. Zenone T. Fever of unknown origin in rheumatic diseases. Infect Dis Clin North Am. 2007;21(4):1115-35, x-xi. https://doi.org/10.1016/j.idc.2007.08.006
2. De Kleijn EM, Vandenbroucke JP, van der Meer JW. Fever of unknown origin (fuo). IA prospective multicenter study of 167 patients with fuo, using fixed epidemiologic entry criteria. The Netherlands fuo Study Group. Medicine (Baltimore). 1997;76(6):392-400. https://doi.org/10.1097/00005792-199711000-00002
3. Valeyre D, Prasse A, Nunes H, Uzunhan Y, Brillet PY, Müller-Quernheim J. Sarcoidosis. Lancet. 2014;383(9923):1155-67. https://doi.org/10.1016/S0140-6736(13)60680-7
4. Thomas KW, Hunninghake GW. Sarcoidosis. jama. 2003;289(24):3300-3. https://doi.org/10.1001/jama.289.24.3300
5. Johns CJ, Michele TM. The clinical management of sarcoidosis: a 50-year experience at the Johns Hopkins Hospital. Medicine (Baltimore). 1999;78(2):65-111. https://doi.org/10.1097/00005792-199903000-00001
6. Iannuzzi MC, Fontana JR. Sarcoidosis: clinical presentation, immunopathogenesis, and therapeutics. JAMA. 2011;305(4):391-9. https://doi.org/10.1001/jama.2011.10
7. Westney GE, Judson MA. Racial and ethnic disparities in sarcoidosis: from genetics to socioeconomics. Clin Chest Med. 2006;27(3):453-62, vi. https://doi.org/10.1016/j.ccm.2006.04.002
8. Al-Kofahi K, Korsten P, Ascoli C, Virupannavar S, Mirsaeidi M, Chang I, et al. Management of extrapulmonary sarcoidosis: challenges and solutions. Ther Clin Risk Manag. 2016;12:1623-1634. https://doi.org/10.2147/TCRM.S74476
9. Chavarriaga-Restrepo A, López-Amaya JE, Mesa-Navas MA, Velásquez-Franco CJ. Sarcoidosis: muchas caras, una enfermedad. Revisión narrativa de la literatura. Iatreia. 2019;32(3):191-203. https://doi.org/10.17533/udea.iatreia.11
10. Santamaría-Alza Y, Fajardo Rivero JE. Sarcoidosis: una serie de casos del nororiente colombiano. Neumol Cir Tórax. 2017;76(1):14-6
11. Muñoz C, Restrepo-Escobar M, Martínez-Muñoz M, Echeverri A, Márquez J, Pinto LF. Differences between patients with sarcoidosis with and without joint involvement treated for fifteen years in a third level hospital. Reumatol Clin. 2020;16(1):45-8. https://doi.org/10.1016/j.reuma.2018.01.001
12. Bautista-Vargas M, Puerta G, Scarpetta-González DF, Marín JD, Salazar-Otoya N, Nieto-Aristizábal I, Aguirre-Valencia D. Epidemiological characterization of patients with sarcoidosis in a high complexity hospital in southwestern Colombia. Rev Colomb Reumatol. 2021. https://doi.org/10.1016/j.rcreu.2021.03.009
13. Chen H, Jin R, Wang Y, Li L, Li K, He Y. The utility of 18F-fdg pet/ct for monitoring response and predicting prognosis after glucocorticoids therapy for sarcoidosis. Biomed Res Int. 2018;2018:1823710. https://doi.org/10.1155/2018/1823710
14. Teirstein AS, Machac J, Almeida O, Lu P, Padilla ML, Iannuzzi MC. Results of 188 whole-body fluorodeoxyglucose positron emission tomography scans in 137 patients with sarcoidosis. Chest. 2007;132(6):1949-53. https://doi.org/10.1378/chest.07-1178
Notas de autor
* Autora de correspondencia: ana.arango@hotmail.com