
ISSN:1692-7273 | eISSN:2145-4507



Empleo de células madre mononucleares en el tratamiento de osteartritis en rodilla: caso de estudio en Cuba
Using Mononuclear Stem Cells for Osteoarthritis-Knee Treatments: A Case Study in Cuba
Uso de células-tronco mononucleares no tratamento da osteoartrite de joelho: estudo de caso em Cuba
Diana Patricia Hermida Vitar, Lourdes Zumalacárregui de Cárdenas, José García Suárez
Empleo de células madre mononucleares en el tratamiento de osteartritis en rodilla: caso de estudio en Cuba
Revista Ciencias de la Salud, vol. 19, núm. 2, 2021
Universidad del Rosario
Diana Patricia Hermida Vitar
Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos, Cuba
 Contribution: conceptualización de la investigación; trabajo experimental; análisis de datos; redactó el informe final
Contribution: conceptualización de la investigación; trabajo experimental; análisis de datos; redactó el informe final
Lourdes Zumalacárregui de Cárdenas * lourdes@quimica.cujae.edu.cu
Universidad Tecnológica de La Habana, Cuba
 Contribution: conceptualización de la investigación; análisis de datos; supervisó el desarrollo del trabajo; responsable de la revisión del informe final
Contribution: conceptualización de la investigación; análisis de datos; supervisó el desarrollo del trabajo; responsable de la revisión del informe final
José García Suárez
Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos, Cuba
 Contribution: análisis de datos; revisión del informe final
Contribution: análisis de datos; revisión del informe final
Recibido: 02 marzo 2020
Aceptado: 03 septiembre 2020
Información adicional
Para citar este artículo: Hermida Vitar DP, Zumalacárregui de Cárdenas L, García Suárez J. Empleo de células madre mononucleares en el tratamiento de osteoartritis en rodilla: caso de estudio en Cuba. Rev Cienc Salud. 2021;19(2):1-15. https://doi.org/10.12804/revistas.urosario.edu.co/revsalud/a.10284
Resumen: Introducción: el desarrollo alcanzado en la medicina regenerativa posibilita el tratamiento de enfermedades incurables o que tienen una respuesta reducida a las terapéuticas actuales, así como la disminución del consumo de medicamentos, en algunos casos. En Cuba, las especialidades de angiología y de ortopedia y traumatología son las que más han aplicado esta terapia. En el artículo se interpretan estadísticamente los resultados de la comparación, mediante STATGRAPHICS® Centurion XVI, de las variables controladas en dos tratamientos de osteoartritis en rodilla, uno empleando células madre mono- nucleares obtenidas de la sangre periférica y otro con la terapia convencional, para fundamentar la superioridad del nuevo tratamiento. Presentación del caso: se trataron 100 pacientes adultos atendidos en el Departamento de Ortopedia del Instituto de Hematología e Inmunología por osteoartrosis de rodilla, divididos en dos grupos. El grupo A (control) recibió el tratamiento convencional de infiltración con acetato de triamcinolona en la articulación afectada. El grupo B (estudio) recibió la implantación del concentrado de células mononucleares adultas hematopoyéticas por vía percutánea. Conclusión: se analizaron cada una de sus variables y se pudo comprobar que la mayoría de los datos recopilados no cumplía con una distribución normal, por lo que las siguientes pruebas se ejecutaron tomando como referencia la mediana de cada muestra. Se comparó entre la evaluación del dolor a la actividad y el consumo de medicamentos de cada uno de los grupos de tratamiento. Se evidenció la mejor respuesta de los pacientes para el tratamiento con células madre y una disminución en el consumo de fármacos.
Palabras clave: terapia celular, células madre, estadística y datos numéricos.
Abstract: Introduction: The development achieved in regenerative medicine has allowed the treatment of incurable diseases or those with a reduced response to current therapies, as well as cases with decreased consumption of medicines. In Cuba, angiology, orthopedic, and traumatology specialists use this therapy the most. In this paper, we have presented the statistical analysis using the STATGRAPHICS® Centurion XVI for controlled variables in two osteoarthritis-knee treatments, one using mononuclear stem cells obtained from the peripheral blood and the other with a conventional therapy so as to demonstrate the superiority of the new treatment regime. Case report: A total of 100 adult patients treated in the Orthopedic Department at the Hematology and Immunology Institute for osteoarthritis-knee pains were studied. Group A (control) received the conventional treatment with triamcinolone acetate infiltration in the affected knee. Group B received the percutaneous implantation of the hematopoietic adult mononuclear cell concentrate. Conclusion: The analysis of each of the variables was performed to verify that most of the collected data did not comply with a normal distribution; hence, the following tests were performed taking the median of each sample as a reference. Comparisons were made between the evaluation of pain to the activity, as well as the consumption of drugs from each of the treatment groups. The best response of the patients was indicated for treatments with stem cells and a decrease in the consumption of drugs.
Keywords: Cell therapy, stem cells, statistical data, numerical data.
Resumo: Introdução: o desenvolvimento alcançado na medicina regenerativa possibilita o tratamento de doenças incuráveis ou que têm uma resposta reduzida frente às terapias atuais, bem como a redução do consumo de medicamentos, em alguns casos. Em Cuba, as especialidades de angiologia e ortopedia e traumatologia são as que mais têm aplicado esta terapia. O estudo interpreta estatisticamente os resultados da comparação, por meio do STATGRAPHICS® Centurion XVI, das variáveis controladas em dois tratamentos de osteoartrite de joelho, sendo um utilizando células-tronco mononucleares obtidas de sangue periférico e outro com terapia convencional, com o objetivo de comprovar a superioridade do novo tratamento. Apresentação do caso: foram tratados 100 pacientes adultos atendidos no Departamento de Ortopedia do Instituto de Hematologia e Imunologia para osteoartrite de joelho, divididos em dois grupos. O grupo A (controle) recebeu tratamento convencional de infiltração com acetato de triancinolona na articulação afetada. O grupo B (estudo) recebeu implantação percutânea de concentrado de células mononucleares hematopoiéticas adultas. Conclusão: a análise de cada uma de suas variáveis foi realizada e constatou-se que a maioria dos dados coletados não obedecia a uma distribuição normal, de modo que os seguintes testes foram realizados tomando-se como referência a mediana de cada amostra. Foram feitas comparações entre a avaliação da dor à atividade, bem como o consumo de medicamentos em cada um dos grupos de tratamento. Evidenciou-se uma melhor resposta dos pacientes ao tratamento com células-tronco e diminuição do consumo de medicamentos.
Palavras-chave: terapia celular, células-tronco, estatísticas e dados numéricos.
Introducción
El trasplante de células y tejidos humanos es un área de la medicina que presenta un fuerte crecimiento y grandes oportunidades para tratar enfermedades, hasta ahora, incurables o con respuesta reducida a las terapéuticas actuales (1,2,3). Ejemplo de estas son las enfermedades neurodegenerativas, las cardiovasculares o la diabetes (4).
Las investigaciones y aplicaciones no clínicas y clínicas de las células madre adultas, en particular las hematopoyéticas, han avanzado mucho, fundamentalmente teniendo en cuenta las dificultades surgidas de la obtención y empleo de las células madre embrionarias, las pluripotentes inducidas (que muestran un riesgo mayor en cuanto a la formación de teratomas) y las de origen fetal perinatal, susceptibles de ser utilizadas autólogamente (5,6). En Cuba, las investigaciones clínicas practicadas hasta el momento con el uso de productos basados en células y tejidos han aportado resultados muy prometedores, principalmente en las especialidades de angiología y de ortopedia y traumatología, que representan el 44.7 % y el 47.1 % de enfermos tratados, respectivamente (7,8).
Desde el inicio de la aplicación de células madre en Cuba, se han estado usando las células mononucleares (CMN) en su conjunto, derivadas de la médula ósea de los propios pacientes, así como las CMN movilizadas a la sangre periférica, luego de la administración de factor estimulador de colonias de granulocitos (filgrastim), como agente movilizador de estas. Las CMN que se han utilizado hasta el momento son autólogas y se basan en procesos y procesamientos simples que incluyen controles en cada una de sus etapas, como su cuantificación, estudio de la viabilidad celular, pruebas microbiológicas y funcionales básicas de los productos y la correspondiente validación y control de calidad (5,9).
Teniendo en cuenta que el mayor porcentaje de pacientes tratados con la terapia celular se ubica en la especialidad de ortopedia y traumatología, se seleccionó el implante de células mononucleares adultas en las lesiones degenerativas de la articulación de la rodilla como caso de estudio, con el objetivo de comprobar si existen diferencias estadísticamente significativas en las respuestas de los pacientes al tratamiento cuando este se realiza con células madre mononucleares y con terapia convencional, en cuanto a la evaluación del dolor a la actividad durante el tiempo de seguimiento y el consumo de fármacos para aliviar el dolor.
Presentación del caso
Se tomó como caso de estudio el tratamiento aplicado a 100 pacientes adultos atendidos en el Departamento de Ortopedia del Instituto de Hematología e Inmunología por osteoartrosis de rodilla, divididos en dos grupos. El grupo A (control) recibió el tratamiento convencional, que consistió en la infiltración con acetato de triamcinolona en la articulación afectada. El grupo B (estudio) recibió la implantación del concentrado de CMN adultas hematopoyéticas por vía percutánea. Para seleccionar a los pacientes estudiados se siguieron los criterios de inclusión y exclusión que se presentan a continuación. La clasificación entre el grupo de control y el grupo de ensayo fue aleatoria. Para los análisis estadísticos se consideró el tamaño de muestra igual al número de rodillas infiltradas en cada tratamiento, de donde el tamaño de la muestra es mayor que el de los pacientes estudiados.
Previo a su inclusión, los pacientes se familiarizaron con el procedimiento y realizaron diferentes movimientos como flexión-extensión, sentarse y llevar tobillo sobre rodilla, que permitió al médico conocer el grado de movimiento de la articulación. Para todos se llevó a cabo un estudio preimplante, que permitiera la selección de la población que se iba a estudiar. Los criterios de inclusión en el estudio fueron: pacientes mayores de 30 años de edad de cualquier sexo con diagnóstico radiológico de lesiones degenerativas de la articulación de la rodilla y pacientes con rango articular adecuado. Una vez seleccionados para el estudio, firmaron el consentimiento informado, que ratifica la inclusión de cada paciente a la investigación.
Los criterios de exclusión del estudio fueron: pacientes con destrucción articular severa, anquilosis articular, anemia que no pueda controlarse por transfusión hasta por encima de 10 g/dL de hemoglobina, pacientes con enfermedades malignas en los últimos 5 años, pacientes que habiendo emitido el consentimiento informado se retractara posteriormente y pacientes con insuficiencia cardiaca, hepática o renal.
Para la caracterización de la población fueron objeto de análisis la edad y el sexo de cada uno de los pacientes tratados. En el procesamiento de los datos se asignó a cada paciente un código numérico con el objetivo de proteger su identidad.
Con los pacientes del grupo B se realizó la movilización de células madre adultas hematopoyéticas, utilizando el factor estimulador de colonias de granulocitos (filgrastim), a dosis de 40 μg por kilogramo de peso, dividido en 4 subdosis de 10 μg por kilogramo de peso cada 12 horas. La última dosis se administró entre tres y seis horas antes de la extracción (10).
Se tomó un hemograma antes de la movilización y a las 3 horas de la última dosis de filgrastim. Si el conteo de leucocitos era mayor de 20 x 109 leucocitos/L y el resto de los parámetros se mantenían normales, se procedía a la extracción de sangre periférica. Si el conteo era menor, se continuaba con la movilización cada 12 horas hasta lograr el conteo de leucocitos antes mencionado.
El número absoluto de CMN se obtuvo mediante su conteo en un contador automático de células. El recuento diferencial se realizó en extensiones del concentrado de CMN en láminas de cristal teñidas con May-Grunwald-Giemsa. Se determinó la viabilidad celular por el método del tripán azul, tanto antes como después de la conservación celular.
Para la identificación de las células madre hematopoyéticas se empleó el marcador CD34+. El recuento se expresó como el porcentaje que se obtuvo mediante citometría de flujo.
A ambos grupos se les hizo seguimiento clínico durante un año a intervalos de tiempo 0, 1, 6 y 12 meses. Para evaluar la respuesta clínica de los pacientes se utilizaron como variables de respuesta la evaluación del dolor a la actividad (EDA) y la frecuencia del tratamiento farmacológico (fTf). Se obtuvo la información mediante intercambio directo con el paciente. Las variables estudiadas, al ser cualitativas, se codificaron de la siguiente manera: EDA en una escala visual analógica de 0 a 100, donde 100 es el máximo dolor (se consideró dolor intenso: 61-100 puntos; moderado: 31-60, y ligero: 0-30 puntos) y fTf (analgésicos, antinflamatorios o ambos) en una escala entre 1 y 4 según la frecuencia de consumo referida por el paciente: siempre para consumo diario, frecuente si consume más de tres veces por semana y ocasional si consume menos de dos veces por semana. La escala aplicada fue siempre: 1 punto; frecuente: 2 puntos; ocasional: 3 puntos, y nunca: 4 puntos.
Se consideró como una respuesta buena la disminución del dolor y del consumo de fármacos a partir de la cuarta semana, manteniéndose hasta los 6 meses.
Adicionalmente, en el grupo B, para conocer la respuesta de los pacientes al tratamiento con células madres se determinaron las variables: porcentaje de células madre mononucleares antes de la movilización (% CMN premov), porcentaje de células madre mononucleares después de la movilización (% CMN posmov), contenido de leucocitos antes de la movilización (CL premov), contenido de leucocitos después de la movilización (CL posmov), porcentaje de células mononucleares en el concentrado (% CMN conc), contenido de leucocitos en el concentrado (CL conc) y concentración de células mononucleares en rodilla (Conc. CMN R).
Los datos se procesaron utilizando el programa STATGRAPHICS® Centurion XVI (11). Mediante su aplicación es posible un análisis descriptivo de una o varias variables, utilizando gráficos que expliquen su distribución o calculando sus medidas características. Cada una de las variables respuesta estudiadas se analizaron tanto para el grupo A como para el grupo B, y a partir de los valores del sesgo estandarizado y la curtosis estandarizada; igualmente, además del ajuste de los datos al gráfico de probabilidad normal, se pudo determinar si la muestra provenía de una distribución normal. Valores de estos estadísticos fuera del intervalo de −2 a +2 indican desviaciones significativas de la normalidad, lo que invalida cualquier prueba estadística con referencia a la desviación estándar.
Para comparar los dos tratamientos se empleó la prueba Mann-Whitney (de Wilcoxon), dado que el análisis de las variables arrojó una distribución no normal. Esta prueba es útil cuando el supuesto de normalidad es cuestionable y no se encuentra una transformación adecuada. La prueba W de Mann-Whitney se ejecutó combinando los pares de muestras que se iban a analizar, ordenando sus datos de menor a mayor y comparando los valores promedio de las dos muestras en los datos combinados.
Se utilizó también la prueba de Kolmogorov-Smirnov, considerando como hipótesis nula que las dos muestras provienen de la misma población. Con esta se calcula la máxima distancia entre las distribuciones empíricas.
Se contrastaron las respuestas a los tratamientos realizados al grupo A y al grupo B en cuanto a la EDA y la fTf en cada caso. Las variables se compararon dentro del mismo grupo de tratamiento para analizar la influencia de tiempo para un mismo tipo de tratamiento y entre los tratamientos. La identificación de estas comparaciones se expresó como: Variable/ Grupo/Mes.
Discusión
En la tabla 1 se presenta una caracterización de la población estudiada. Se aprecia el predominio de las mujeres, comportamiento que coincide con el de Cruz-Sánchez et al., que lo atribuye a que las mujeres son más propensas a la afección degenerativa, debido a factores hormonales y por la osteoporosis más temprana (12). Se observó la presencia mayoritaria de la afectación en ambas rodillas, tanto para el grupo control como para el grupo de intervención. La edad promedio en el grupo control fue ligeramente superior a la de los miembros del grupo de intervención, para un nivel de significación de 0.05.
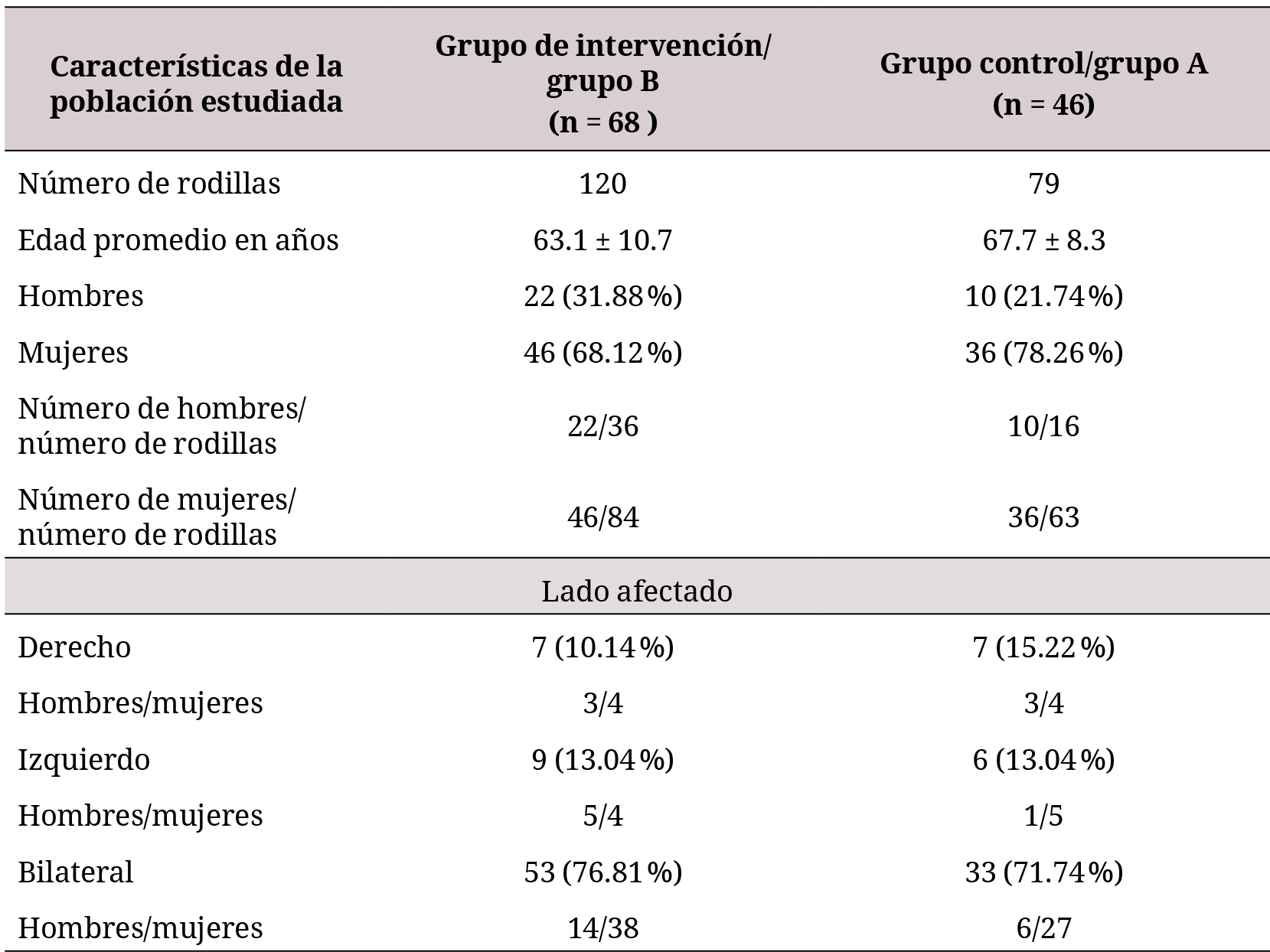
Análisis de cada variable
En la tabla 2 se reportan los estadígrafos para las variables estudiadas en el grupo B. Se comprobó que todas, excepto el porcentaje de células madre mononucleares antes de la movilización (media = 38.21; desviación estándar = 10.03) y el contenido de leucocitos en el concentrado (media = 308.33 Χ 109 leucocitos/L; desviación estándar = 151.25 X 109 leucocitos/L), no cumplían con una distribución normal. De ahí los altos valores de sesgo y curtosis estandarizados que se obtienen para las variables %CMN posmov, CL premov, CL posmov, % CMN conc y Conc. CMN R.
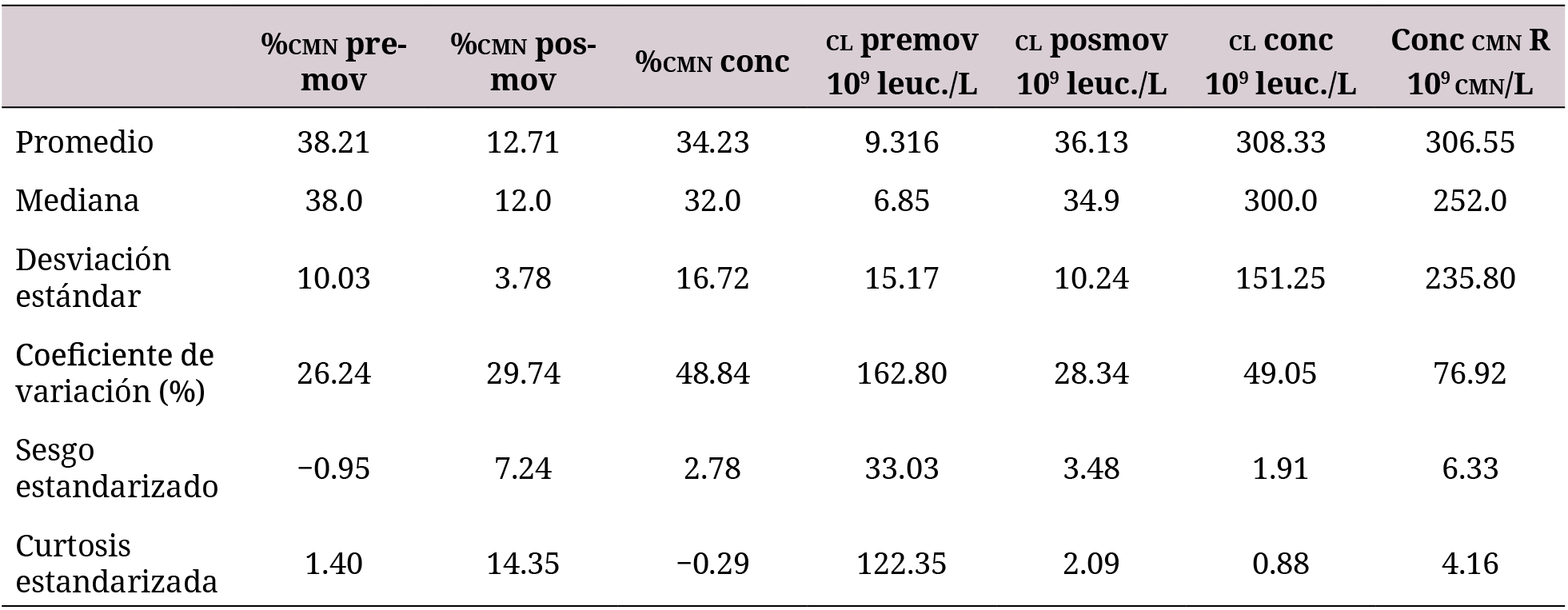
Por otra parte, se aprecia el alto valor de coeficiente de variación de la variable CL premov, lo cual depende de cada organismo. Para la extracción de sangre periférica se esperó a que el conteo de leucocitos fuera mayor de 20 x 109 leucocitos/L, lo que justifica la reducción del coeficiente de variación de la variable CL posmov. El uso de un factor estimulador de colonias de granulocitos como filgrastim estimula la movilización de las células madre hematopoyéticas mediante la disminución de la expresión del gen del SDf-1α y de las concentraciones de proteínas, a la vez que aumentan las proteasas que pueden romper las interacciones entre las células madre hematopoyéticas y el ambiente de la médula ósea (10).
En la tabla 2 se aprecia el incremento del contenido de leucocitos después de la movilización, con una mediana de 34.9 x 109 leucocitos/L, superior al 20 x 109 leucocitos/L, establecido como control de la etapa de movilización. El valor medio del contenido de leucocitos en el concentrado es inferior al reportado por Cruz-Sánchez et al., de 523.15 ± 59.24 x 109/L, al seguir un procedimiento similar (12). En la tabla 3 se muestra el resumen estadístico para la EDA del grupo A y del grupo B para diferentes tiempos.
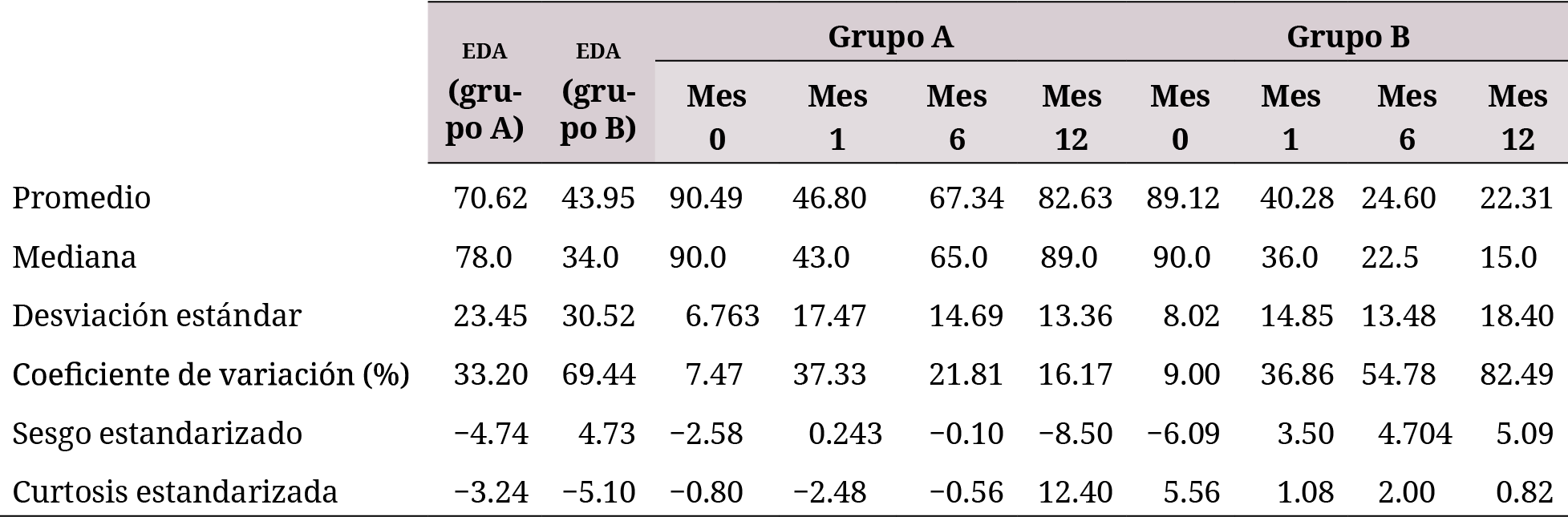
Los valores de sesgo estandarizado de la tabla 3 se encuentran fuera del intervalo esperado para datos provenientes de una distribución normal, con excepción de los meses 1 y 6 del grupo A. Para la curtosis estandarizada los resultados de la EDA para el grupo A en los meses 0 y 6 y para el grupo B al mes 1, 6 y 12 presentan valores que se encuentran en el intervalo de una distribución normal. No obstante, con la combinación de ambos estadígrafos solo el mes 6 del grupo A presentan valores en el intervalo de normalidad.
De la integración de las tablas 2 y 3 se aprecia que con los valores estadísticos mostrados se puede plantear que la mayoría de las muestras no provienen de una distribución normal. Por eso, la comparación entre los resultados obtenidos con los tratamientos del grupo A y del grupo B tomaron como referencia la mediana de dichas muestras y no su media.
Comparación entre variables
EDA A vs. EDA B
En el histograma que se representa en la figura 1 se puede observar la frecuencia con la que aparecen los resultados atendiendo a la escala de dolor descrita.
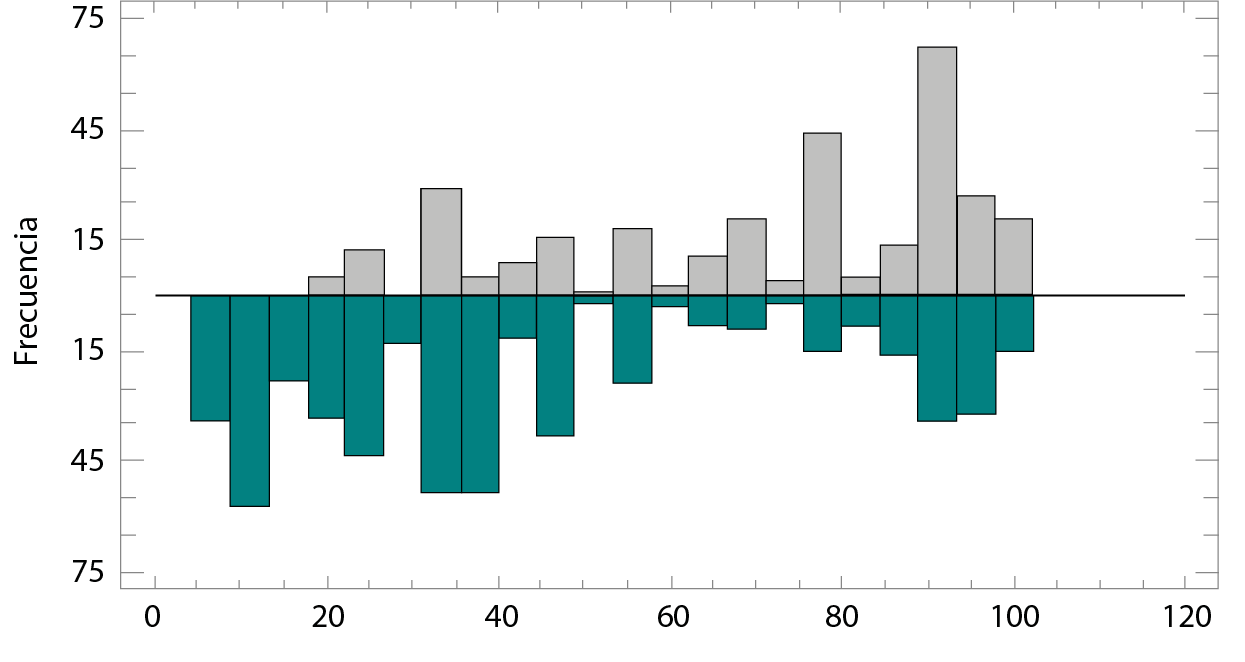
Para el grupo A, las observaciones de la EDA A se encuentran en el intervalo de 21 a 99 y las barras más altas, o sea, las de mayor frecuencia, de 75-80 y de 90-95. El intervalo del EDA B estuvo entre 5 y 99 y la mayor frecuencia apareció entre los valores 10-15 y 30-35. Esto quiere decir que para el grupo A las mayores frecuencias corresponden a valores en los que el dolor es intenso; todo lo contrario, para el grupo B, en el que la mayoría reporta valores de dolor ligero.
EDA A y EDA B por mes de seguimiento
En la tabla 4 se presentan los intervalos en los que se movió la frecuencia de observaciones para cada uno de los grupos, en función del tiempo de seguimiento.
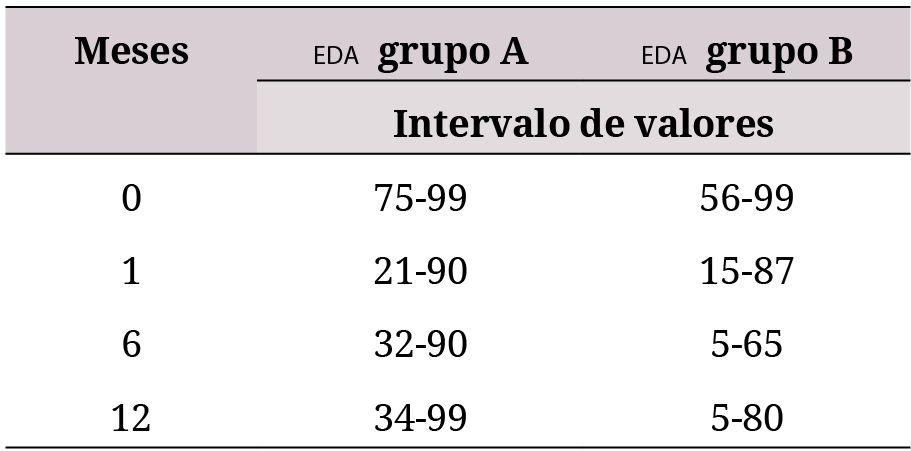
A partir del análisis de las tablas 3 y 4 se aprecia que tanto para los pacientes del grupo A como para los del grupo B se refleja una respuesta favorable al tratamiento, aunque la mejoría del grupo B parece ser más notable. Esto es, al mes de aplicado el tratamiento, la variable EDA ha pasado de la categoría dolor intenso a moderado para ambos grupos. Para el grupo A, en el sexto mes se comienza a observar una recaída del paciente y ya para el control anual se puede decir que se encuentra en el mismo estado que estaba antes de comenzar el tratamiento. Entre tanto, para el grupo B se alcanza la categoría de dolor ligero en la evaluación al sexto mes, y permaneció así para la evaluación al año.
La confirmación de las apreciaciones comentadas se presenta en la tabla 5, que muestra el resultado de la aplicación de las pruebas de Wilcoxon y Kolmogorov-Smirnov, para las variables contenido de leucocitos y porcentaje de CMN, antes de la movilización con filgrastim (premov y posmov) y después de esta para el caso del tratamiento del grupo B. También se presentan los resultados obtenidos de la EDA en el grupo A y en el grupo B, de acuerdo con el tiempo de seguimiento y la comparación para un mismo tiempo entre los resultados de ambos tratamientos.
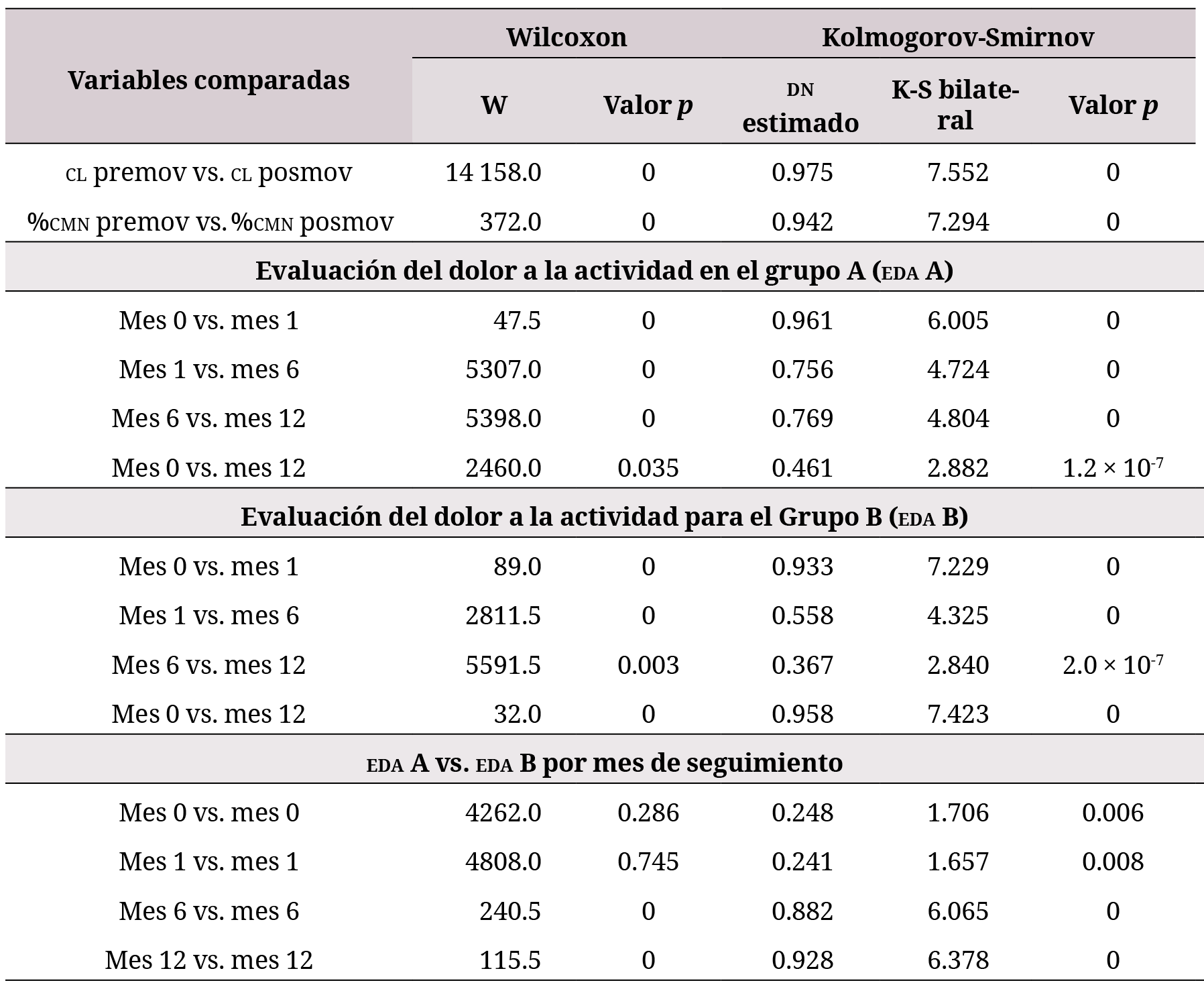
Comparación entre las variables contenido de leucocitos y porcentaje de células mononucleares antes de la movilización con filgrastim y después
Teniendo en cuenta el valor de . reportado por la prueba Wilcoxon en la tabla 5, inferior a 0.05, se puede plantear que existe una diferencia estadísticamente significativa entre las medianas comparadas para ambos grupos, con un nivel de confianza del 95 %.
La prueba de Kolmogorov-Smirnov da distancias máximas muy similares en cada uno de los análisis. De particular interés es el valor de p aproximado para la prueba de cada comparación, los cuales resultaron menores que 0.05, por lo que se afirma que existen diferencias estadísticamente significativas entre las dos distribuciones con un nivel de confianza del 95 %.
Comparación de la evaluación del dolor a la actividad para ambos grupos de tratamiento
edA A de acuerdo con el tiempo de seguimiento. Entre las medianas de estas muestras existe una diferencia estadísticamente significativa con un nivel de confianza del 95 %, debido a que el valor de . es menor que 0.05, así como para las distribuciones acumuladas. De estos resultados se puede destacar que para el mes 0 vs. el mes 12 se observa un aumento en el valor de p, y esto se podría relacionar con la recaída que tienen los pacientes, que se explicó anteriormente.
edA B de acuerdo con el tiempo de seguimiento. Para este grupo también existe una diferencia estadísticamente significativa entre las muestras con un nivel de confianza del 95 %, debido a que el valor de p es menor que 0.05; así como para las distribuciones acumuladas de estas. Nótese que para el mes 6 vs. el mes 12, aunque según el resultado existe una diferencia significativa entre las dos distribuciones con un nivel de confianza del 95 %, los valores en que se mueven los intervalos son similares, de donde lo que da un criterio de que la mejoría alcanzada tiende a una estabilidad.
edA A vs. edA B por mes de seguimiento. La prueba W de Mann-Whitney realizada para comparar las medianas de las muestras reportó un valor de . para el mes 0 vs. el mes 0 y el mes 1 vs. el mes 1 mayor que 0.05 en cada caso, por lo que no existen diferencias estadísticamente significativas entre las mismas con un 95 % de confianza. Para el mes 6 vs. el mes 6 y el mes 12 vs. el mes 12, sí hay diferencias estadísticamente significativas.
Por lo anterior, de acuerdo con los reportes de las comparaciones al inicio de ambos tratamientos, la mayoría de los pacientes de cada grupo padecen un dolor intenso, según la escala para su evaluación. Al mes, ambos declaran padecer de menos dolor al comparar con el estado inicial. Esta mejoría es similar para ambos tratamientos. Al año se aprecia que los pacientes del grupo A se encuentran prácticamente en el mismo estado que al comenzar el tratamiento; sin embargo, los del grupo B presentan una mejoría significativa.
Las comparaciones de las distribuciones de las muestras, ejecutando pruebas de Kolmogorov-Smirnov, arrojaron que, para todos los casos, existe una diferencia estadísticamente significativa entre las dos distribuciones, con un nivel de confianza del 95 %, ya que todos los valores de . fueron menores que 0.05.
A partir de los resultados obtenidos hasta el momento, se plantea que el tratamiento aplicado al grupo B resultó más efectivo que el del grupo A, al lograrse niveles de dolor ligero para el grupo B que se mantienen a partir de los 6 meses, lo que no sucede con el grupo A, en que llegado a valor moderado comienza a subir el valor en la escala del dolor.
En un estudio con nueve pacientes tratados con células madres, Lugo et al. refieren que al mes de tratamiento el 100 % de los pacientes refirió no tener dolor (13). Por su parte, Cruz-Sánchez et al. indicaron que el dolor articular se redujo significativamente, ya que al inicio del estudio todos los pacientes (n = 123) presentaron dolor de moderado a insoportable; mientras que a los seis meses solo 21 tuvieron esta clasificación del dolor, y en el resto desapareció o solo estuvo de manera ligera (12). Esta rápida mejoría después de la terapia celular, aunque refieren que no hay una explicación definitiva, sugieren que está relacionada con la liberación por las CMN implantadas de citocinas con actividad antinflamatoria. También pudiera relacionarse con la capacidad regenerativa de las células implantadas, o bien por la asociación de ambos mecanismos de acción.
Como resultado, Lamo-Espinosa et al. obtuvieron que el uso de las células madres resulta en una disminución significativa del dolor que se mantiene al menos un año (14). Además, es independiente de la dosis administrada en el tratamiento. En el grupo control no se apreciaron diferencias entre el inicio y el final del tratamiento al año. En esencia, los resultados de estos tres estudios se corresponden con los obtenidos en el presente trabajo.
Comparación del consumo de medicamento para aliviar el dolor para ambos grupos de tratamiento
En la figura 2a se observa una reducción del consumo de medicamento en los pacientes del grupo B, al comparar el tiempo cero con la evolución en el seguimiento del año. En cambio, para los pacientes del grupo A, prácticamente, se mantienen igual, lo cual se demuestra en el histograma de frecuencia de la figura 2b.
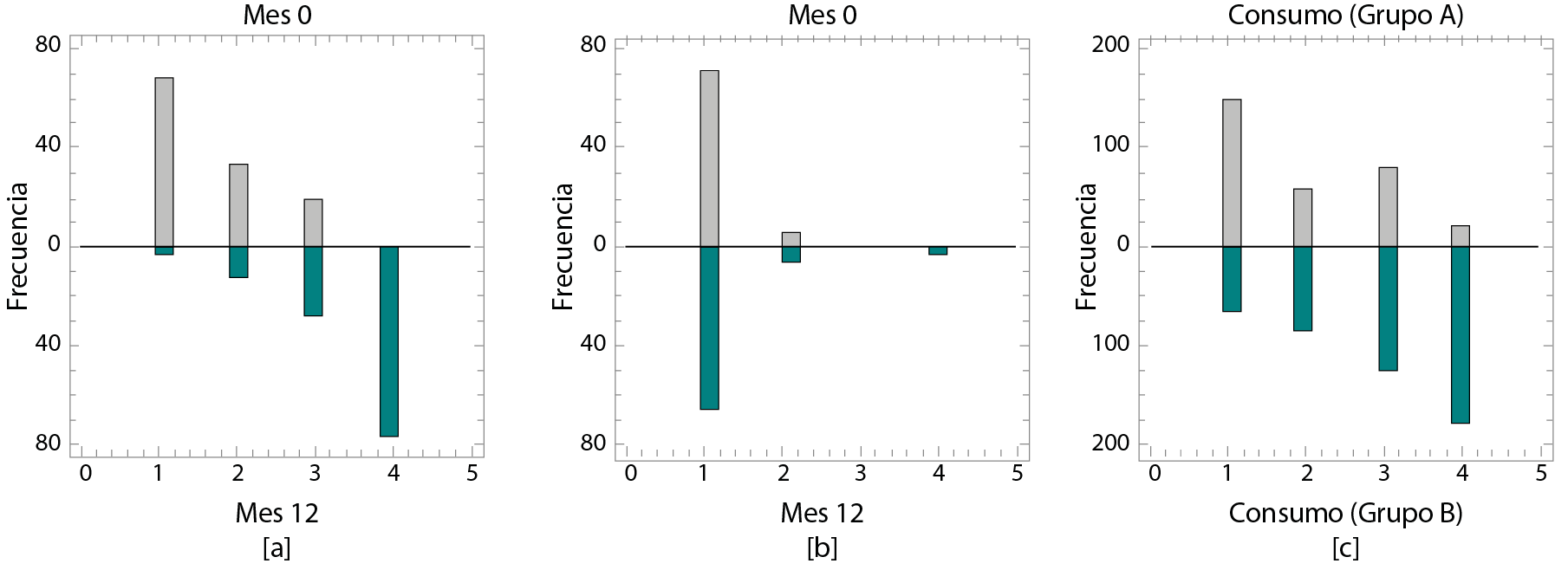
Este comportamiento era de esperar, teniendo en cuenta los resultados obtenidos al analizar la EDA. Para los pacientes del grupo B la mejoría fue considerable, lo que conlleva una disminución del consumo de medicamentos para aliviar el dolor. Sin embargo, para el caso del grupo A, en el que el dolor permanece al año del tratamiento, el paciente necesita analgésicos y antinflamatorios que permitan el alivio a la hora de realizar sus actividades.
Al comparar los histogramas de ambos grupos, se obtuvo que existen diferencias estadísticamente significativas con un nivel de confianza del 95 %. Este resultado se encuentra estrechamente relacionado con los resultados obtenidos en las comparaciones de la EDA, por lo que el comportamiento se puede considerar similar. Los mejores resultados se obtienen para los pacientes del grupo B, lo cual se puede apreciar en los histogramas de frecuencia de la figura 2c. Al contrastar ambos tratamientos, teniendo en cuenta todos los reportes del análisis estadístico, se puede plantear que el tratamiento con células es más efectivo que los tratamientos convencionales con esteroides.
Contribución de los autores
Diana Patricia Hermida Vitar realizó la conceptualización de la investigación, el trabajo experimental, el análisis de datos y redactó el informe final.
Lourdes Zumalacárregui de Cárdenas realizó la conceptualización de la investigación y el análisis de datos, supervisó el desarrollo del trabajo y fue la responsable de la revisión del informe final.
José García Suárez participó en el análisis de datos y en la revisión del informe final.
Conflicto de intereses
Ninguno declarado.
Agradecimientos
A la Dra. Aymara Baganet Cobas, por el suministro de la información requerida para el estudio.
Referencias
1. Prósper F, Gavira JJ, Herreros J, Rábago G, Luquin R, Moreno J, Robles JE, Redondo P. Trasplante celular y terapia regenerativa con células madre. An Sist Sanit Navar. 2006;29(supl. 2):219-34.
2. Directiva 2004/23/Ce del Parlamento Europeo y del Consejo de 31 de marzo de 2004 relativa al establecimiento de normas de calidad y de seguridad para la donación, la obtención, la evaluación, el procesamiento, la preservación, el almacenamiento y la distribución de células y tejidos humanos.
3. Food and Drug Administration. Human cells, tissues, and cellular and tissue-based products; establishment registration and listing, 21 CfR Parts 207, 807, and 1271 [internet]. 2001 ene 19. Disponible en: https://www.federalregister.gov/documents/2001/01/19/01-1126/human-cells-tissues-and-cellular-and-tissue-based-products-establishment-registra-tion-and-listing
4. Estopá-Dueso J. Aspectos científicos, técnicos y éticos de la terapia celular y medicina regenerativa [tesis doctorado]. León: Universidad de León; 2013.
5. Hernández-Ramírez P, Forrellat Barrios M. Ventajas de la terapia celular con células mononucleares derivadas de la médula ósea, aplicadas en su conjunto. Rev Cubana Hematol Inmunol Hemoter. 2013;29(4):407-12.
6. Picón-Ruiz M. Aislamiento y caracterización de células madre/progenitoras y tumorales humanas: potencial terapéutico e implicaciones en carcinogénesis [tesis de doctorado]. Granada: Universidad de Granada; 2012.
7. Hernández-Ramírez P. Medicina regenerativa y células madre: resultados con el uso de componentes de la sangre. Documento procedente de la Jornada Científica de Medicina Regenerativa; 2015; La Habana, Cuba.
8. Roque L, Alfonso Y, Plaín C. Aplicaciones de las células madre en la angiología cubana. Revista Universidad Médica Pinareña. 2018;14(3):276-88.
9. Feito T, Perurena C, Aparicio JL, Bustillo MJ, García F. Implante de células madre hematopoyéticas en pacientes con isquemia crónica de los miembros inferiores. Rev Cuba Angiol Cir Vasc. 2015;16(1):64-75.
10. Camacho J, Camacho L, Gómez N, Camacho A, López K, García L. Células madre: generalidades (parte II). Mediciego. 2017;23(3):35-44.
11. Statgraphics® Centurion XVI. StatPoint Technologies, Inc. 2009. EE. UU.
12. Cruz-Sánchez P, Gámez-Pérez A, Rodríguez-Orta C, González Y, López E, Pérez D, et al. Impacto del tratamiento con células madre adultas en la osteoartrosis de la rodilla. Rev Cubana Hematol Inmunol Hemoter. 2013;29(3):272-83.
13. Lugo A, Arce M, Hernández V, Díaz A, Díaz M. Medicina regenerativa en el tratamiento de la osteoartrosis de rodilla: experiencias en Villa Clara. Medicent Electrón. 2015;19(3):171-3.
14. Lamo-Espinosa J, Mora G, Blanco J, Granero F, Núñez-Córdoba J, Sánchez-Echenique C, et al. Intra-articular injection of two different doses of autologous bone marrow mesenchymal stem cells versus hyaluronic acid in the treatment of knee osteoarthritis: multicenter randomized controlled clinical trial (phase I/II). J. Transl Med. 2016;14:246. https://doi.org/10.1186/s12967-016-0998-2
Notas de autor
* Autora de correspondencia: lourdes@quimica.cujae.edu.cu



