

Un caso de carcinoma de tiroides de células de Hürthle. Abordando la incertidumbre del papel del Yodo I-131
A case of Hürthle Cell Thyroid Carcinoma. Dealing with the Uncertainty of the Role of Iodinel-131
Um caso de carcinoma de tireoides de células de Hürthle. Abordando a incerteza do papel do Iodo I-131
Un caso de carcinoma de tiroides de células de Hürthle. Abordando la incertidumbre del papel del Yodo I-131
Revista Ciencias de la Salud, vol. 15, núm. 1, 2017
Universidad del Rosario
Recibido: 11 Septiembre 2015
Aceptado: 17 Agosto 2016
Información adicional
Para citar
este artículo: Gutiérez-Villamil C, Francisco-Alonso
J, Mejía-López A, Carofilis-Mendoza F, Arévalo-Leal JS,
Marín-Oyaga V. Un caso de carcinoma de tiroides de
células de Hürthle. Abordando la incertidumbre del
papel del Yodo I-131. Rev Cienc
Salud. 2017;15(1):165-172. Doi: https://doi.org/10.12804/revistas.urosario.edu.co/revsalud/a.5388
Jacqueline
Mugnier, patóloga: Todos ellos prestan sus servicios
en la Fundación Cardioinfantil – Instituto de Cardiología
de Bogotá, Colombia.
Descargos de responsabilidad: La financiación del trabajo se realizó con recursos propios y no
hubo otras fuentes. Los autores no declaran conflictos de interés. La
responsabilidad de los conceptos que se publican es íntegramente de los
autores.
Resumen: Objetivo: el fin de este artículo es dar a conocer la experiencia del manejo multidisciplinario de un caso documentado de carcinoma de células de Hürthle en el que se encontró captación con I-131 y por lo tanto opción terapéutica con el mismo. Presentación de caso: se trata de una paciente en la sexta década de la vida, diagnosticada inicialmente con bocio difuso quien fue manejada con terapia de sustitución hormonal con análogos de tiroxina sin respuesta satisfactoria, por lo que se realizó biopsia tiroidea, cuyo resultado reportó neoplasia de células de Hürthle de comportamiento inespecífico. Se realizó tiroidectomía oncológica y linfadenectomía. Se realizó revisión de placas de patología y se llegó a un diagnóstico definitivo de carcinoma de Hürthle. Se llevó el caso a junta multidisciplinaria y se decide terapia con I-131 pero este proceso llevó a que la terapia se realizara de forma tardía; aun así se evidencia en el rastreo postratamiento, captación en adenopatía cervical. Finalmente, presentó recaída pulmonar 12 meses después. Este tipo de tumor es un desafío para los médicos tratantes por la incertidumbre en su historia natural, en su tratamiento y en la utilidad del I-131, esta última es muy debatida debido a su alta tendencia a la desdiferenciación y al bajo porcentaje de los mismos que presentan captación del radiofármaco. Es incierto si la paciente de este caso se hubiese podido beneficiar de una terapia ablativa con I-131 más temprana disminuyendo el riesgo de recaída luego de haberse documentado avidez tumoral por el mismo.
Palabras clave: carcinoma de células de Hürthle, glándula tiroides, radioisótopos de yodo.
Abstract: Objetive: The objective is to present a case with successful I-131 uptake in a patient with Hürthle cell carcinoma. Case presentation: A 60 years old female patient with diagnosed goiter, that was treated with thyroid hormone analogues that didn’t decreased the growth of the mass; due to that, it was biopsied. The report of the pathology reported a Hürthle cell neoplasm with indeterminate behavior, lately oncologic thyroidectomy and lymphadenectomy were performed, from which the pathology plates were revised showing a definitive diagnosis of Hurthle cell carcinoma. The case was reviewed in a medical board where I-131 therapy was suggested. In the postheraphy scan performed, there was evidence of I-131 uptake in the neck and in an adenopathy. Twelve months later, there was evidence of pulmonary relapse. Is an uncertainty to know if the patient in this case would have been able to benefit from an early ablative therapy with I-131 decreasing the risk of relapse after having documented tumor avidity for it. The Hürthle thyroid carcinoma is rare, and its natural history is still controversial because it’s challenging diagnosis, treatment and monitoring. Because there is no definitive agree about his integral approach despite it has been considered differentiated thyroid cancer even therapy with I-131 is still debated.
Keywords: Hurthle cell thyroid cancer, thyroid gland, iodine radioisotopes.
Resumo: Objetivo: O fim deste artigo é dar a conhecer a experiência do manejo multidisciplinar de um caso documentado de carcinoma de células de Hürthle no qual encontrou-se captação com I-131 e pelo tanto opção terapêutica com o mesmo. Presentación de caso: Trata-se de uma paciente na sexta década da vida, diagnosticada inicialmente com bócio difuso que foi tratada com terapia de substituição hormonal com análogos de tiroxina sem resposta satisfatória, pelo que se realizou biopsia tireóidea, cujo resultado reportou neoplasia de células de Hürthle de comportamento inespecífico. Realizou-se tireoidectomia oncológica e linfadenectomia. Realizou-se revisão de placas de patologia e chegou-se a um diagnóstico definitivo de carcinoma de Hürthle. Levou-se o caso à junta multidisciplinar e decide-se terapia com I-131 mas este processo levou a que a terapia se realizara de forma tardia; ainda assim evidencia-se no rastreamento pós-tratamento captação em adenopatia cervical. Finalmente, apresentou recaída pulmonar 12 meses depois. Este tipo de tumor pe um desafio para os médicos tratantes pela incerteza na sua história natural, no seu tratamento e na utilidade do I-131, esta útlima é muito debatida devido à sua alta tendência à desdiferenciação e à baixa percentagem dos mesmos que apesentam captação do radiofármaco. É incerto se a paciente deste caso se tivesse conseguido beneficiar de uma terapia ablativa com I-131 mais temporã diminuindo o risco de recaída após ter-se documentado avidez tumoral pelo mesmo.
Palavras-chave: Carcinoma de células de Hürthle, glândula tireoides, radioisótopos de iodo.
Introducción
El tumor de células de Hürthle debe su nombre al histólogo alemán Karl Hürthle y fue citado por James Ewing en 1919 quien maximizó la difusión de este término, usado exclusivamente para la neoplasia oncocítica tiroidea. Sin embargo, el primero en describir estas células fue Max Azkenazy y por ello se puede encontrar en la literatura con este epónimo, también llamado oncocítico u oxifílico indistintamente. El carcinoma de células de Hürthle (CCH) es un tipo raro de tumor tiroideo maligno en el que se producen cambios celulares que constan de la acumulación en masa de mitocondrias, cuya morfología muchas veces está alterada. Estos cambios celulares suelen presentarse en enfermedades inflamatorias o que producen estrés celular similar sin necesidad de implicar malignidad, como la enfermedad de Graves, la tiroiditis linfocítica crónica, el bocio nodular o la exposición de la glándula a radiación, y puede considerarse normal su hallazgo en ancianos e incluso en otros órganos. Los cambios de las células de Hürthle se relacionan con el metabolismo oxidativo y la producción de radicales libres. Se ha relacionado la aparición de este tipo de tumores con deleciones del ADN mitocondrial y mutaciones puntuales como en el gen GRIM-19 (1, 2).
El grupo etario de mayor prevalencia del CCH se encuentra entre los 50-60 años y su diagnóstico patológico es considerado todo un reto, así como la diferenciación entre lesiones benignas y malignas. Adicionalmente, hay controversia acerca de la clasificación patológica y el manejo de este tipo de tumor. La OMS (Organización Mundial de la Salud) y otros grupos como la ATA (American Thyroid Association) lo clasifican dentro del grupo de tumores diferenciados foliculares de tiroides dentro de las guías de manejo y seguimiento; otros como la AFIP (Armed Forces Institute of Pathology) sugieren clasificarlo como otro tipo de tumor tiroideo y en contraste, la NCCN (National Comprehensive Cancer Network) dedica un capítulo aparte a los carcinomas papilares, foliculares (que son ávidos por I-131 y por lo tanto suceptibles de tratamiento) y del anaplásico (no ávido por I-131 y no suceptible de tratamiento) para manejo propio del CCH, debido probablemente a su mayor agresividad comparado con los otros tipos de carcinomas diferenciados de tiroides. De igual forma, el tratamiento del CCH con I-131 es controversial, aunque se ha demostrado que puede prolongar el tiempo libre de progresión de la enfermedad y la mejoría en la supervivencia. Lo anterior está sujeto a un diagnóstico e intervención tempranos, ya que el CCH tiende a desdiferenciarse rápidamente, tener baja captación por el I-131 y, por consiguiente, hacerse resistente al tratamiento isotópico; si bien no existen tiempos determinados debería actuarse con la mayor prontitud posible para realizar la yodoterapia en pacientes con CCH (3, 4, 5, 6, 7, 8, 9, 10).
Presentamos un caso de CCH que es inicialmente diagnosticado como un tumor oncocítico de comportamiento indeterminado y posteriormente reportado como maligno, en el que en principio se realizó únicamente manejo quirúrgico. Cuando se confirma malignidad se discute interdisciplinarimente la posibilidad de terapia con I-131, la cual se administró a pesar de ser tardíamente, por la evidencia de incremento progresivo de la tiroglobulina obteniendo captación positiva del mismo que, sin embargo, presentó recaida posterior. Se pretende entonces discutir el potencial beneficio que hubiese tenido el haber dado tratamiento isotópico con antelación en este y otros casos.
Presentación del caso
Paciente de género femenino, de 63 años de edad, fumadora, sedentaria e hipertensa sin antecedente de exposición a radiaciones ni antecedentes familiares de importancia, a quien se le diagnosticó bocio e hipotiroidismo manejado inicialmente con análogos de hormona tiroidea. Por ausencia de respuesta a la terapia y crecimiento de bocio, se consideró realización de biopsia por aspiración con aguja fina (ACAF) sobre nódulo tiroideo que reportó “lesión folicular de comportamiento a establecer”, por lo que se realizó tiroidectomía total con linfadenectomía. El reporte de patología posquirúrgico lo reportó como “tumor oncocítico multifocal sin invasión capsular, dos ganglios linfáticos peritiroideos con hiperplasia folicular reactiva”. Fue manejada con suplencia de hormona tiroidea y seguimiento. Dos años después, en una ecografía de control, se encontró masa en cuello en lecho tiroideo de 17x12x23mm sin adenomegalias, que fue enviado a biopsia y reportó tumor de células oncocíticas; se realizó tomografía computarizada (TC) en la que se informa que dicha masa corresponde a una metástasis ganglionar (masa hipodensa paratraqueal) por lo que se le realizó nueva linfadenectomía cervical cuya patología reportó “nódulo tiroideo de patrón oncocítico sin otras especificaciones” y siete ganglios libres de tumor y radiograía de tórax normal.
La paciente es posteriormente valorada por la junta multidisciplinaria de tiroides de la institución, quienes solicitan revisión de las placas de patología de la tiroidectomía y el vaciamiento ganglionar inicial, donde se reporta: “carcinoma de células de Hürthle metastásico”. Al mismo tiempo, los valores del marcador tumoral: tiroglobulina, que venía siendo negativa durante el seguimiento, inició incremento con valor final de 17.6 ng/ml (TSH: 0,1 mUI/ml) con anticuerpos antitiroglobulina negativos. En la reunión multidisciplinaria, se discute entre los participantes la controversia de la administración o no de terapia con I-131 (debido a la incertidumbre de la utilidad y efectividad del tratamiento isotópico por la baja probabilidad de captación), que finalmente es aceptada por el grupo y se realiza con dosis de 100 mCi bajo protocolo de estimulación con tirotropina alfa (TSHrh) sin complicaciones. El rastreo corporal total realizado cinco días posterapia evidenció captación focal correspondiente a adenopatía metastásica en la estación cervical III derecha y fue negativo para lesiones metastásicas yodocaptantes a distancia (figuras 1-2). Laboratorios luego de la estimulación con TSHRH: TSH 30.78 mUI/ml, tiroglobulina 19.68 ng/ml y anticuerpos anti-tiroglobulina, negativos.
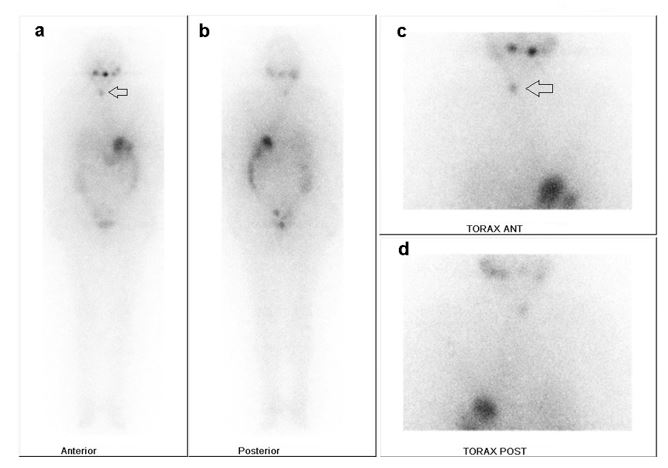
Se muestra imagen de cuerpo completo en proyecciones anterior (a) y posterior (b) donde se observa distribución normal del I-131 por glándulas salivares hipercaptantes y presencia por saliva radiactiva en boca. Existen escasa actividad hepática y en tracto gastrointestinal. La flecha señala la adenopatía cervical en fase de irradiación. Imágenes sectoriales en proyecciones anterior (c) y posterior (d) de región de interés. La flecha señala la adenopatía cervical en fase de irradiación.
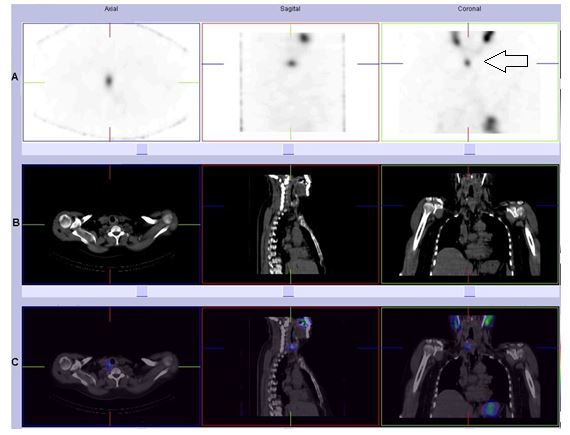
Figura 2. A: Imágenes en planos axial, sagital y coronal de spect. La flecha en detalle apunta al tejido tiroideo en fase de irradiación. B: Imágenes en planos axial, sagital y coronal de ct. C: Imágenes en planos axial, sagital y coronal de fusión spect-ct.
En los meses posteriores al tratamiento, los niveles de tiroglobulina se encuentran en aumento progresivo por lo que se realiza ecografía de cuello a los 4 meses posterapia sin evidencia de lesiones. Se continuaron realizando controles bimensuales en los que persistía el aumento paulatino de los niveles de tiroglobulina sin presentar cambios clínicos y a los nueve meses posterapia, realizan TC de cuello que no encuentra anormalidades y TC de tórax en la que se evidencian nódulos subcentimétricos en el lóbulo superior del pulmón izquierdo y en el lóbulo medio. La gammagrafía ósea es negativa para metástasis. Ante dichos hallazgos se realiza tomografía por emisión de positrones/tomografía computarizada con fluorodesoxiglucosa (18F-FDG-PET/CT), que muestra nódulos pulmonares subcentimétricos hipermetabólicos (sugestivos de malignidad) de distribución aleatoria, que alcanzan un standard uptake value máximo de 13 (suvmax elevado) y adenopatías cervicales de aspecto reactivo. Por dichos hallazgos y casi triplicación de los niveles de tiroglobulina (niveles finales de 173 ng/ml con TSH de 0,2 mUI/ ml) se revisa nuevamente en junta, en donde a pesar de la alta sospecha de desdiferenciación tumoral, pero por antecedente de avidez por I-131, se decide nuevo tratamiento isotópico de rescate con 150 mCi de I-131 bajo protocolo de estimulación con TSHrh. No se consideró necesario concepto del comité ético de la institución. En el rastreo posterapia no se evidenciaron lesiones yodocaptantes indicando definitivamente desdiferenciación tumoral sobre enfermedad incialmente diferenciada, lo que redujo considerablemente las opciones terapéuticas.
Discusión
El CCH es considerado un tipo raro de tumor tiroideo diferenciado, que oscila entre un 3-7% de todos los tumores tiroideos según se ha reportado. Dicho porcentaje varía dados los factores epidemiológicos de cada muestra en los grupos de estudio. En Colombia, la prevalencia del CCH no está muy documentada pero recientemente un grupo multidisciplinario reportó su existencia y encontró que corresponde tan solo al 2.2% de todos los tipos de cáncer de tiroides en un seguimiento institucional de 1997 a 2012. Tiene una relación de 3:1 de mujeres sobre hombres y su prevalencia es mayor en las décadas quinta y sexta de la vida. Como se mencionó previamente, el CCH presenta incertidumbre actual acerca de su clasificación patológica, historia natural y tratamiento. En este caso se expone la realidad actual en la forma de abordaje del CCH como un tumor tiroideo diferenciado que comparte algunos aspectos de comportamiento y pronóstico propios de este grupo de tumores y así son clasificados por importantes organizaciones como la OMS y la ATA. Sin embargo, la evidencia reciente sugiere que el CCH posee características histológicas y de evolución distintas a los tumores diferenciados propiamente dichos que implican una mayor agresividad, sobrevida más corta y finalmente necesidad de otro tipo de tratamiento. Dichas características constituyen la base fundamental para justificar un tratamiento más temprano y agresivo (1, 3, 4, 7, 8, 11, 12).
En el caso descrito, el personal médico se enfrentó a un reto diagnóstico como es habitual en el CCH para determinar la malignidad de la lesión oncocítica, decidir la conducta quirúrgica y discutir la pertinencia o no de la terapia con I-131 debido a los conceptos contradictorios acerca de la misma. Se dice que solo un bajo porcentaje de los CCH captan I-131, y que este oscila entre el 5-10% y adicionalmente dicha captación disminuye en los paciente mayores de 40 años, soportándose en la hipótesis que el CCH tiende a desdiferenciarse rápidamente perdiendo la capacidad de captar yodo. En el caso presentado, se documentó en el rastreo posterapia con I-131 captación en adenopatía cervical tardía respecto al diagnóstico inicial. En el seguimiento, la paciente evolucionó a progresión de la enfermedad con lesiones pulmonares metastásicas y desdiferenciación definitiva. La inquietud que queda planteada es ¿qué tanto puede contribuir la administración tardía de la terapia isotópica con I-131 con respecto al diagnóstico inicial en el avance rápido del tumor hacia la aparición de lesiones metastásicas y desdiferenciación, teniendo en cuenta que entre más temprano es instaurado el tratamiento existe una mejor respuesta y sobrevida? Tal vez la incertidumbre mencionada acerca de la implementación del I-131 en pacientes con este tipo de tumores debido a la sospecha de que no van a tener captación por el radiofármaco haya retrasado justificadamente su uso en este caso particular en el que posteriormente se observó que, aunque tardíamente, sí había captación(1, 3, 4, 8, 13).
Queda entonces abierto el considerar la terapia temprana con I-131 en casos individualizados como parte integral del tratamiento del CCH así como protocolos de tratamiento específicos para dicha patología. Sin embargo, aún no existen suficientes estudios que demuestren o refuten cómo predecir la desdiferenciación celular y el probable papel curativo temprano del I-131 en el CCH.
Agradecimientos
Agradecimientos especiales por su aporte incondicional y su soporte multidisciplinar permanente al Dr. Gabriel Sánchez de Guzmán, cirujano de cabeza y cuello; al Dr. Alex Valenzuela, endocrinólogo, y a la Dra.
Referencias
1. Sandoval MA, Paz-Pacheco E. Hürthle cell carcinoma of the thyroid. BMJ Case Rep. 2011.
2. Maximo V, Lima J, Prazeres H, Soares P, Sobrinho-Simoes M. The biology and the genetics of Hürthle cell tumors of the thyroid. Endocr Relat Cancer. 2012;19(4):R131-47.
3. Paliogiannis P, Attene F, Scognamillo F, Marras V, Losa F, Trogu F, et al. Management of thyroid Hürthle cell neoplasms: A single centre experience and literature review. Europ J Oncol. 2012(17):181-8.
4. Cannon J. The significance of Hürthle cells in thyroid disease. Oncologist. 2011;16(10):1380-7.
5. American Thyroid Association (ATA) Guidelines Taskforce on Thyroid Nodules and Differentiated Thyroid Cancer, Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009;19(11):1167-214.
6. Chindris AM, Casler JD, Bernet VJ, Rivera M, Thomas C, Kachergus JM, et al. Clinical and molecular features of Hürthle cell carcinoma of the thyroid. J Clin Endocrinol Metab. 2015;100(1):55-62.
7. Goffredo P, Roman SA, Sosa JA. Hürthle cell carcinoma: a population-level analysis of 3311 patients. Cancer. 2013;119(3):504-11.
8. Barnabei A, Ferretti E, Baldelli R, Procaccini A, Spriano G, Appetecchia M. Hürthle cell tumours of the thyroid. Personal experience and review of the literature. Acta Otorhinolaryngol Ital. 2009;29(6):305-11.
9. Tuttle RM, Haddad RI, Ball DW, Byrd D, Dickson P, Duh QY, et al. Thyroid carcinoma, versión 2.2014. J Natl Compr Canc Netw. 2014;12(12):1671-80.
10. Nagar S, Aschebrook-Kilfoy B, Kaplan EL, Angelos P, Grogan RH. Hürthle cell carcinoma: an update on survival over the last 35 years. Surgery. 2013;154(6):1263-71.
11. Lopez-Penabad L, Chiu AC, Hoff AO, Schultz P, Gaztambide S, Ordoñez NG, et al. Prognostic factors in patients with Hurthle cell neoplasms of the thyroid. Cancer. 2003;97(5):1186-94.
12. Sánchez G, Gutiérrez C, Valenzuela Á, Tovar JR. Differentiated carcinoma of the thyroid: Findings after 16 years of multidisciplinary management. Rev Col Cir. 2014;29(2):102-9.
13. Hanief MR, Igali L, Grama D. Hürthle cell carcinoma: diagnostic and therapeutic implications. World J Surg Oncol. 2004;2(27).
Notas de autor
1 MD
2 MD
3 MD
4 MD
5 MD, PhD
6 MD, MSc
vmarin@cardioinfantil.org