10.12804/revistas.urosario.edu.co/revsalud/a.14826
ARTÍCULOS DE INVESTIGACIÓN CLÍNICA O EXPERIMENTAL
Hernán Ariolfo Álvarez Berrezueta, Lcdo., Enf.1*
Sabrina Lisseth Chapa Chapa, Lcda. Enf.2
1 Centro de Salud Tipo B Achupallas (Ecuador).
 0000-0002-3373-9552
0000-0002-3373-9552
 hernanalvarex@outlook.com
hernanalvarex@outlook.com
2 Centro de Salud Tipo B Achupallas (Ecuador).
 0000-0001-8783-7097
0000-0001-8783-7097
Recibido: 9 de septiembre de 2024
Aprobado: 24 de enero de 2025
Para citar este artículo: Álvarez Berrezueta HA, Chapa Chapa SL. Inhibidores de la bomba de protones y cáncer pancreático: revisión sistemática de estudios observacionales analíticos. Rev Cienc Salud. 2025;23(1):1-17. https://doi.org/10.12804/revistas.urosario.edu.co/revsalud/a.14826
Resumen
Introducción: el cáncer de páncreas representa un grave problema de salud, pues es la séptima causa de mortalidad en el mundo y muestra una clara tendencia al aumento; por
esto, es fundamental identificar factores de riesgo predictivos, como la
relación propuesta entre los inhibidores de la bomba de protones y el
desarrollo de cáncer pancreático, a fin de implementar estrategias rentables
de prevención y detección temprana.
Objetivo: determinar la asociación
entre el uso de inhibidores de la bomba de protones y el desarrollo de cáncer
pancreático a partir de estudios observacionales analíticos.
Materiales y métodos: revisión sistemática de la literatura científica, bajo los
criterios de la declaración prisma. Se buscó en las bases de datos Pudmed, ScienceDirect y Scopus.
Resultados: se obtuvieron 954 artículos, tras
aplicar criterios de inclusión y exclusión. En la revisión se incluyeron un
total de 7 estudios, de los cuales se valoró el riesgo de sesgo bajo la escala Newcastle-Ottawa; la relación causal, a través de los criterios de Bradford Hill, y se analizó temporalidad, dosificación y categorización, siendo la causalidad
inversa, una inexistente gradiente biológica y de temporalidad, resultados
heterogéneos, causalidad y tamaño de efecto débiles, características
cuestionables presentes en los estudios valorados.
Conclusión: no existe un respaldo sólido bajo la revisión de la evidencia entre
posibles efectos carcinogénicos y páncreas a causa del uso de
inhibidores de la bomba de protones. Es imperante desarrollar ensayos
controlados aleatorizados para dilucidar resultados.
Palabras clave: neoplasias pancreáticas; inhibidores de la bomba de protones; farmacoepidemiología.
Abstract
Introduction: Pancreatic cancer currently represents a serious health problem. It is the seventh leading cause of mortality worldwide and the incidence of pancreatic cancer shows a
clear upward trend. Therefore it is essential to identify predictive risk
factors, such as the proposed relationship between proton pump inhibitors and
the development of pancreatic cancer, in order to implement cost-effective
strategies for prevention and early detection. The aim of the present study was
to determine the association between the use of proton pump inhibitors and the
development of pancreatic cancer from analytical observational studies.
Materials and methods: A systematic review of the scientific literature was carried
out under the criteria of the PRISMA statement, the search was performed in PudMed, ScienDirect and Scopus.
Results: A total of 954 articles were obtained, after applying the inclusion and exclusion criteria, a total of 7 studies were included in the review, the risk of bias was assessed
under the Newcastle-Ottawa scale, the causal relationship through the Bradford
Hill criteria and temporality, dosage and categorization were analyzed, being
the inverse causality, a non-existent biological and temporality gradient,
heterogeneous results, weak causality and effect size, questionable
characteristics present in the assessed studies.
Conclusion: There is no
solid support under review of the current evidence between possible pancreatic
carcinogenic effects due to the use of proton pump inhibitors; therefore, it is
imperative to develop randomized controlled trials to elucidate the results.
Keywords: pancreatic neoplasm; proton pump inhibitors; pharmacoepidemiology.
Resumo
Introdução: o câncer de pâncreas representa atualmente um grave problema de saúde e é a sétima principal causa de mortalidade em todo o mundo. O de câncer de pâncreas mostra clara tendência de aumento, o que torna essencial a identificação de fatores de risco preditivos, como a relação proposta entre os inibidores da bomba de prótons e o desenvolvimento de câncer de pâncreas, a fim de implementar estratégias custo-efetivas de prevenção e detecção precoce. Nesse sentido, o objetivo do presente estudo é determinar a associação entre o uso de inibidores da bomba de prótons e o desenvolvimento de câncer de pâncreas a partir de estudos observacionais analíticos.
Materiais e métodos: realizou-se uma revisão sistemática da
literatura seguindo os critérios da declaração PRISMA. A busca foi feita no PubMed, na ScienceDirect e no Scopus.
Resultados: inicialmente foram identificados 954 artigos. Após a aplicação dos critérios de inclusão e exclusão, sete estudos foram selecionados para a revisão. O risco de viés foi avaliado pela escala de Newcastle-Ottawa. A relação causal foi avaliada com base nos critérios de Bradford Hill, e aspectos
como temporalidade, dosagem e categorização foram analisados. Houve resultados heterogêneos, causalidade fraca e tamanho do efeito com características questionáveis nos estudos avaliados. Além disso, não foram observados causalidade reversa, gradiente biológico e de temporalidade.
Conclusão: a revisão das evidências atuais não fornece suporte sólido para a associação entre o uso de inibidores da bomba de prótons e possíveis efeitos carcinogênicos no pâncreas. Estudos controlados e randomizados são necessários para elucidar essa relação.
Palavras-chave: neoplasias pancreáticas; inibidores da bomba de prótons; farmacoepidemiologia.
Introducción
En el mundo, el cáncer de páncreas (CAP) es una de las principales causas de muerte por cáncer; de hecho, ocupa el séptimo lugar y su carga global ha logrado duplicarse en los últimos 25 años (1). En 2017, hubo 441 000 casos de cap, en comparación con 196 000 evidenciados en 1990 (2). Las regiones con mayor incidencia de CAP incluyen América del Norte, Europa y Australia (3); es más, en Estados Unidos se considera la tercera causa de mortalidad relacionada con el cáncer y se proyecta a convertirse en la segunda en 2030 (4).
Es inusual la detección temprana y los avances en tratamientos oncológicos no han logrado conseguir un éxito aceptable en prolongar la supervivencia. De hecho, se ha documentado una relación mortalidad-incidencia del 94 % (5), pues más del 80 % de los pacientes se presentan con la enfermedad en estadio avanzado, lo que genera una tasa de supervivencia de 5 años en tan solo el 11 % de estos casos (6). Aparte de lo anterior, el riesgo de muerte por CAP aumenta drásticamente con la edad; se han evidenciado 2 decesos por cada 100 000 pacientes en menores de 40 años y 90 en mayores de 80 años (7).
Dado su gran impacto mundial, es fundamental la identificación clara de factores de riesgo predictivos con la posterior implementación de estrategias rentables de prevención y detección temprana, para reducir no solo el estrés fisiológico en los pacientes con CAP, sino también la carga de ingresos al sistema de salud pública. Bajo esta premisa, un grupo de fármacos, denominados inhibidores de la bomba de protones (IBP), se han visto relacionados con cuadros de carcinogénesis secundaria a hipergastrinemia compensatoria en modelos experimentales en animales y cultivos celulares (8-10). Esto aunado a que a finales de la década de 1990 y principios de los 2000 se evidenció el aumento de uso de IBP, debido a la creciente incidencia de trastornos relacionados con el ácido gástrico, una tendencia que se mantiene hasta la fecha.
En efecto, la incidencia anual de prescripciones de IBP aumentó del 19.7 % en 2012 a un 23.0 % en 2017 (11), hasta el punto de llegar a dominar el tratamiento de supresión ácida y encontrarse entre los medicamentos más recetados en todo el mundo (12). De hecho, uno de cada cuatro adultos que acudieron a consulta médica recibieron una prescripción de un IBP en 2017 (13); sin embargo, algunas veces se han utilizado en indicaciones preventivas y no autorizadas, con una justificación no del todo clara y sin evidencia que respalde su uso (14,15). Pese a los beneficios y la buena tolerancia, ha persistido la preocupación frente a la exposición especialmente prolongada a este grupo de medicamentos, y ya se ha advertido sobre su asociación con un mayor riesgo de fracturas, absorción deficiente de magnesio, vitamina B12 y otros minerales (12,16,17). Empero, la evidencia clínica disponible para la mayoría de los efectos secundarios es débil o contradictoria, y los beneficios del tratamiento con IBP parecen superar los posibles efectos adversos. Por lo anterior, el objetivo de esta revisión sistemática fue determinar la asociación entre el uso de IBP y el desarrollo de CAP, basándose en estudios observacionales analíticos recientes.
Materiales y métodos
Se llevó a cabo una revisión sistemática de la literatura científica en torno a la relación del uso de IBP y el desarrollo de CAP, bajo los criterios de la declaración PRISMA (18), para la adecuada ejecución de revisiones sistemáticas. La búsqueda se dio en el periodo comprendido entre febrero y abril de 2024, en las bases de datos Pudmed, ScienceDirect y Scopus, en las que se usaron los siguiente términos de búsqueda, junto con los operadores booleanos pertinentes: case control study AND cohort study AND pancreatic cancer AND proton pump inhibitor OR dexlansoprazole OR esomeprazole or lansoprazole OR omeprazole OR pantoprazole OR rabeprazole. Se establecieron los siguientes parámetros de inclusión y exclusión:
Criterios de inclusión: los estudios seleccionados fueron observacionales analíticos, ya fueran de casos y controles o de cohorte, en cuyo resultado principal se buscó el análisis de la relación de causalidad entre usuarios de IBP y el desarrollo de CAP. Se incluyeron también estudios en idioma inglés y español y que se hubieran publicado entre 2013 y 2023.
Criterios de exclusión: los artículos que no incluyeron estudios en humanos, los estudios con participantes menores de 18 años, los estudios en los que los participantes contaran con antecedentes de cáncer, los ensayos controlados aleatorios, los estudios cualitativos, las revisiones y los artículos de opinión de expertos. También se excluyeron resúmenes y disertaciones no arbitradas.
Evaluación del riesgo de sesgo y causalidad en los estudios incluidos
La calidad de los estudios se valoró mediante la Escala Newcastle-Ottawa (19), misma que se encuentra compuesta por tres dominios: la selección de los participantes del estudio, la comparabilidad de los grupos y la determinación del resultado de interés o desenlace, aplicables a estudios de casos y controles o de cohortes. La puntuación total es 9 y una puntuación de 7 o más indica un estudio de alta calidad.
Por otro lado, se emplearon los criterios de Bradford Hill para evaluar la relación causal y aplica una valoración bajo 9 criterios: fuerza de asociación, gradiente biológico, temporalidad, consistencia, experimentación, coherencia, plausibilidad, analogía y especificidad. La puntuación total se calculó como la suma del número de criterios que se cumplieron, para obtener una calificación de entre 0 y 3, 4 y 6, 6 y 9, lo que indica: causalidad débil, moderada y fuerte, respectivamente (20). Es pertinente resaltar que no se contactó con ningún autor para aclaraciones pertinentes; por ende, solo se valoró el material publicado para medir el riesgo de sesgo.
Resultados
En esta revisión sistemática se identificaron un total de 953 artículos mediante su búsqueda profunda y según los criterios establecidos en las bases de datos: 12 artículos en Pubmed, 715 artículos en ScienceDirect y 226 artículos en Scopus. Se utilizó EMBASE y Web of Science, que dieron como resultado la adición de un estudio. Luego de eliminar artículos por duplicidad, se obtuvieron 926; de estos, se excluyeron 876 tras leer el título y 42 tras leer el resumen. De los 8 artículos restantes sometidos a revisión de texto completo, se eliminó uno, por no contar con información completa tanto en el aspecto metodológico como en los resultados. Finalmente, quedaron 7 estudios para la revisión sistemática. La figura 1 corresponde al proceso de selección según PRISMA.
Figura 1. Uso de la metodología prisma para la selección de estudios
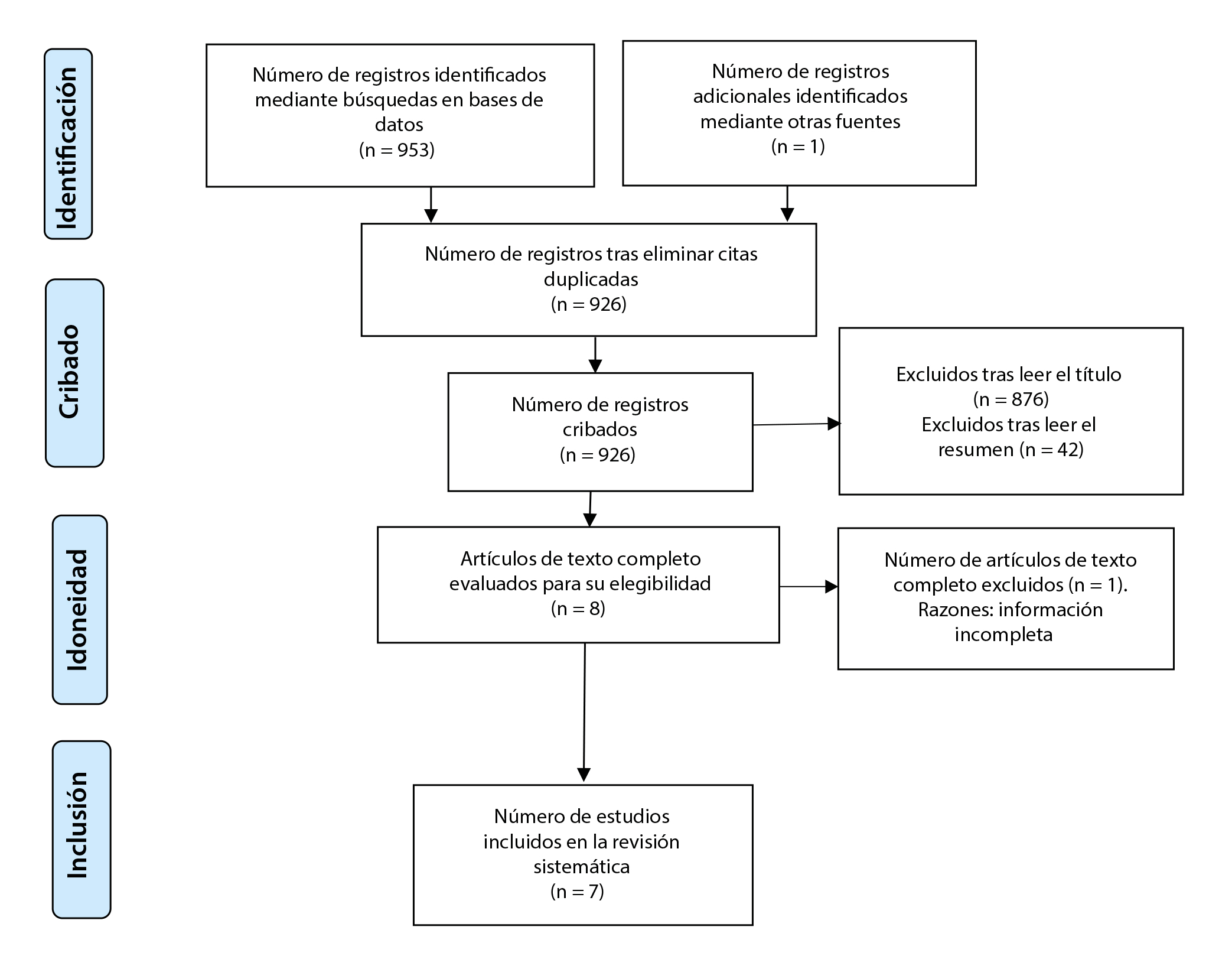
Los datos se extrajeron y sintetizaron en la tabla 1. La calidad de los estudios se evidencia en la tabla 2 y la valoración de causalidad bajo los criterios de Bradford Hill se encuentra en la tabla 3.
Tabla 1. Resumen de información y resultados de estudios sobre uso de inhibidores de la bomba de protones y desarrollo de cáncer de páncreas
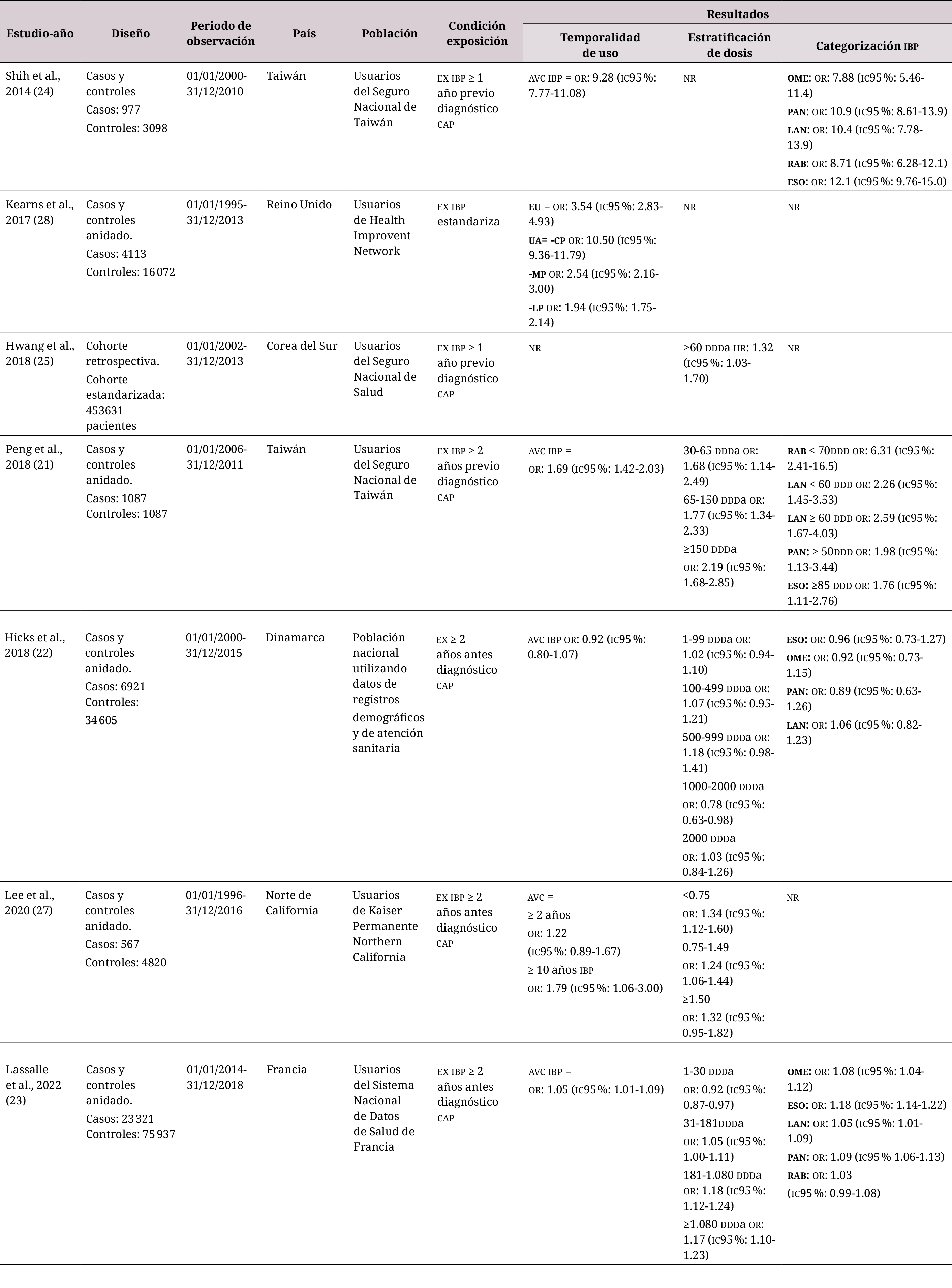
EX: exposición, IBP: inhibidores de la bomba de
protones, CAP: cáncer de páncreas, AVC alguna vez consumió. EU: exusuarios (prescripción de inhibidores de la bomba de protones más reciente mayor a 6 meses antes del diagnóstico de cáncer de páncreas). UA: usuarios activos (prescripción más reciente de inhibidores de la bomba de protones menor 6 meses antes del diagnóstico de cáncer de páncreas). CP: corto plazo (primera prescripción menor a 12 meses previo diagnóstico de cáncer de páncreas), MD: mediano plazo (primera prescripción entre 12 y 24 meses previo diagnóstico de cáncer de páncreas). LP: largo plazo (primera prescripción mayor o igual a 24 meses previo diagnóstico de cáncer de páncreas). DDDa: dosis diaria definida acumulativa. P/D: pildoras por día. OME: omeprazol. LAN: lansoprazol. ESO: esomeprazol. RAB: rabeprazol. PAN: pantoprazol. NR: no reporta.
≥ : mayor o igual que. <: menor que. =: igual. or: odds ratio, HR: hazard ratio.
Tabla 2. Valoración de calidad de estudios, mediante parámetros de la escala Newcastle-Ottawa
Estudio |
Selección |
Comparabilidad |
Exposición/ |
Conclusión |
Shih et al., 2014 (24) |
xx |
x |
xx |
Riesgo moderado |
Kearns et al., 2017 (28) |
xxx |
x |
xxx |
Bajo riesgo |
Hwang et al., 2018 (25) |
xxx |
x |
xxx |
Bajo riesgo |
Peng et al., 2018 (21) |
xxx |
xx |
xxx |
Bajo riesgo |
Hicks et al., 2018 (22) |
xxx |
xx |
xxx |
Bajo riesgo |
Lee et al., 2020 (27) |
xxx |
xx |
xxx |
Bajo riesgo |
Lassalle et al., 2022 (23) |
xxx |
xx |
xxx |
Bajo riesgo |
Tabla 3. Valoración bajo criterios de Bradford Hill
Criterios |
Descripción de valoración y evaluación |
Puntaje |
Fuerza de asociación |
Fuerza de la asociación en la estimación del efecto. |
1 |
Gradiente biológico |
Dosis monótona o duración de relación entre la exposición y resulta- do. Visible únicamente en el estudio de Peng et al. (21). |
1 |
Temporalidad |
Relación temporal entre exposición y resultado (exposición precede al resultado, dudosa por causalidad inversa). |
0 |
Consistencia |
Reproducibilidad de asociación propuesta entre informes (resultados heterogéneos). |
0 |
Experimentación |
La propuesta de asociación es apoyada por estudios de laboratorio o clínico aleatorizado ensayos (no en modelos humanos). |
0 |
Coherencia |
Coherencia entre historia natural y biología de la enfermedad (limitada). |
0 |
Plausibilidad |
Explicación para asociación propuesta biológicamente plausible (limitada). |
0 |
Analogía |
Características similares de efectos bajo exposiciones analógicas. Únicamente valorado por Lasalle et al. (23). |
1 |
Especificidad |
Resultado basado únicamente en la exposición (limitada por la etiología multifactorial). |
0 |
Total |
3 |
En el análisis de los estudios implicados en esta revisión sistemática, la edad media de los casos osciló entre 60 y 70 años. Incluso Peng et al. (21) señalan como factor de riesgo con significancia estadística el encontrarse en una edad mayor o igual a los 65 años (OR: 1.25; IC95 %: 1.01-1.55). En estudios donde se realizó una categorización de los diferentes IBP (20-23), el omeprazol figura como el medicamento mayormente recetado, con excepción del artículo realizado por Shih et al. (24), en el cual el esomeprazol toma este papel.
Hubo tres estudios (21-23) en los que se valoró como variable adicional o comparador activo el uso de antagonistas del receptor de la histamina 2 (H2RA), y se encontró únicamente en el artículo de Lassalle et al. (23) una relación estadísticamente significativa entre H2RA y el desarrollo de CAP (OR: 1.55; IC95 %:1.15-2.18), con una dosis diaria definida acumulativa (DDDa) mayor a 1.080. Este mismo estudio se caracteriza por la segmentación en cuanto a la ubicación anatómica de la presentación de la neoplasia maligna, mostrando una frecuencia mayoritaria en la cabeza, con un 53 %; seguido de los originados en el cuerpo del páncreas, con un 13.8 % del total de casos desarrollados.
Cabe destacar que cuatro estudios valoraron la DDDa (21-23,25), misma calculada según la dosis diaria definida. Una de las principales unidades de medida en estudios farmacoepidemiológicos y que corresponde a la dosis media diaria de mantenimiento de un medicamento respecto a la durabilidad del tratamiento pertinentemente abordado, es decir, valorar la dosis total en proporción de temporalidad (26). Así, en el estudio realizado por Hicks et al. (22), por ejemplo, una exposición mayor a 1000 DDDa se entiende como un tiempo de ingesta de un IBP, en dosis de mantenimiento, durante más de tres años. Por su parte, Lee et al. (27) utilizan la medición en pildoras por día para este fin.
Discusión
En la presente revisión sistemática, seis de siete estudios analizados aluden a cierta asociación entre el uso de IBP y el desarrollo de cap. El proceso patológico por el cual se propone este hecho radica en la hipergastrinemia secundaria a una retroalimentación negativa por el uso prolongado de estos medicamentos, lo que podría estimular el crecimiento excesivo de células pancreáticas e inhibir la apoptosis (28,29) y llevar a una alteración de la microbiota intestinal, condición no solo ligada a la génesis, sino también al desarrollo y resistencia a la terapia del CAP (30-32).
En el estudio realizado por Kearns et al. (28) se encontró un número desproporcional de usuarios de IBP a corto plazo en el grupo casos en relación con el control, lo que concurría en resultados secundarios a causalidad inversa (33,34). En efecto, en las últimas décadas se han reportado innumerables casos de asociaciones que se presumían como sólidas, contradichas posteriormente en grandes ensayos de quimioprevención (35); esto dado por los largos periodos de latencia en muchos cánceres, como en el CAP, el cual abarca entre los 8.4 y los 15 años (36,37). Ello le infiere un crecimiento mucho más lento en comparación con otros tumores malignos (38).
En los estudios aquí evaluados, como esfuerzo cuestionable para permitir la latencia, se valoró como exposición el antecedente de consumo de uno o dos años de IBP previos a la fecha del diagnóstico, datos que no satisfacen el proceso de carcinogénesis en correspondencia con la exposición de riesgo. Solamente Lee et al. (27) evidenciaron una ventana de análisis más amplia con una relación positiva pero aún cuestionable mayor o igual a 10 años. Del mismo modo, inherente a este punto de posible sesgo, ninguno de los estudios valorados estratificó el estadio de cáncer en el momento del diagnóstico, lo que sería útil para valorar de una mejor manera el sesgo aparente de causalidad inversa.
Cuatro estudios muestran una valoración de DDDa, teniendo en cuenta este factor. Se podría establecer una relación dosis-respuesta; no obstante, pese a ello, en estudios epidemiológicos, las estimaciones de asociación entre una exposición y los resultados de una enfermedad suelen estar sesgadas cuando se ignoran las incertidumbres de la exposición (39). Por ejemplo, en el estudio de Peng et al. (21) un paciente pudo haber iniciado terapia de IBP con duración de un mes, interrumpir el tratamiento un intervalo de tiempo indeterminado y volver a reanudar dicha terapia dos meses de forma adicional, lo que lo convertiría en un usuario cuya exposición total sería mayor o igual a 150 DDDa. Por su parte, en el estudio realizado en Taiwán (24), donde se enmarca una relación de riesgo por el hecho de asegurar alguna vez el consumo, también pone en tela de juicio la fiabilidad del resultado, caracterizado por una inexistente gradiente biológica y de temporalidad, visible también en tres estudios más (22,23,27), donde la variabilidad a la exposición no sigue un patrón directamente proporcional. Así que se presenta una valoración de riesgo según una variable dicotómica: sí/no consumió alguna vez IBP.
Para el caso de esta regresión logística binaria, se propone una interpretación del or basada en una transformación de la d de Cohen, según la cual si el OR es menor a 1.68, su tamaño del efecto se considera insignificante (1.68-3.47: pequeño; 3.48-6.71: moderado, y mayor a 6.7: grande) (40,41). Bajo esta misma lupa, el sistema Grading of Recommendations, Assessment, Development and Evaluation (GRADE) considera fuerte asociación los hallazgos de or mayores a 2 (42), característica evaluada también en los criterios de causalidad de Bradford Hill (43,44). Así, bajo la valoración de dichos parámetros, los resultados de los estudios aquí abordados muestran una causalidad y evidencia débil. Cabe destacar que estos basan la medida de consumo en canjes sin la garantía de que el paciente cumpla con el régimen terapéutico establecido o que si quiera este haya tomado la medicación, tampoco se tiene en cuenta el IBP usado de venta libre.
Existen factores secundarios, denominados covariables o factores de confusión (45,46). La obesidad, el alcoholismo y el tabaquismo, por ejemplo, fueron condiciones no valoradas en tres estudios (21,22,24), pese a ser catalogadas como factores de riesgo importantes para el desarrollo de CAP (3,47-51). Otro ejemplo claro se puede encontrar en el artículo de Peng et al. (23), en el cual la hepatitis viral tanto B como C (52-54) reflejaron una prevalencia diez veces mayor a lo observado en otro artículo.
Tres estudios analizados se desarrollaron en países asiáticos, y tal parece que el origen étnico desempeña un papel importante en la patogénesis del cap. De hecho, de 1990 a 2019, la tasa de incidencia y mortalidad en Asia marcó un aumento anual promedio del 1.73 % (55) y entre los estadounidenses de origen asiático fue de 5.74 por cada 100000 personas al año (56). Esto es plausible debido a alteraciones patógenas propias de la línea germinal, presentes en asiáticos, como variaciones en BRCA2, PALB2 y SPINK1 (57). Además de ello, son metabolizadores lentos de los IBP, como resultado de una menor expresión del citocromo p450 hepático. Es más, el gen CYP2c19, cuyo alelo sin función más común, CYP 2c19*2, tiene una frecuencia alélica del 30 % en asiáticos, en otros la función es disminuida o nula, como el CYP 2c19*3-*8, y suelen comprender prevalencias del 2 % al 7 %, considerablemente alta. Ello da como resultado una enzima con actividad disminuida (58,59), claro ejemplo de una injerencia determinante que sobrestimará y errará la relación entre el CAP y el uso de IBP.
Conclusión
Esta revisión sistemática encuentra que, aun cuando se identificó una mayor cantidad de estudios que vinculan el uso de IBP con el desarrollo de CAP, los resultados heterogéneos en cuanto a dosis y temporalidad de uso, sesgos importantes aunados a la causalidad débil, demuestran que no existe un respaldo sólido bajo la revisión de la evidencia actual entre posibles efectos de carcinogénesis pancreática, debido al consumo de IBP; sin embargo, es imperante desarrollar ensayos controlados aleatorizados para dilucidar resultados.
Contribución de los autores
Hernán Ariolfo Álvarez Berrezueta: conceptualización, análisis formal-técnicas estadísticas, análisis de datos, metodología-diseño y desarrollo, administración del proyecto-gestión y coordinación, supervisión y liderazgo en la planificación, validación-verificación, redacción-revisión y edición.
Sabrina Lisseth Chapa Chapa: curación de datos, adquisición de fondos, investigación-proceso de investigación, recursos-suministro de materiales de estudio, sofware-programación, diseño e implementación, visualización-presentación de datos, redacción-documento original.
Financiación
Los autores refieren no contar con ningún tipo de financiación.
Conflicto de intereses
Ninguno declarado.
Referencias
1. Partyka O, Pajewska M, Kwasniewska D, Czerw A, Deptala A, Budzik M, et al. Overview of pancreatic cancer epidemiology in Europe and recommendations for screening in high-risk populations. Cancers. 2023;15(14):3634. https://doi.org/10.3390/cancers15143634
2. Pourshams A, Sepanlou S, Ikuta K, Bisignano C. The global, regional, and national burden of pancreatic cancer and its attributable risk factors in 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol. 2019;4(12):934-47. https://doi.org/10.1016/S2468-1253(19)30347-4
3. Klein AP. Pancreatic cancer epidemiology: understanding the role of lifestyle and inherited risk factors. Nat Rev Gastroenterol Hepatol. 2021;18(7):493-502. https://doi.org/10.1038/s41575-021-00457-x
4. Rahib L, Smith BD, Aizenberg R, Rosenzweig AB, Fleshman JM, Matrisian LM. Projecting cancer incidence and deaths to 2030: the unexpected burden of thyroid, liver, and pancreas cancers in the United States. Cancer Res. 2014;74(11):2913-21. https://doi.org/10.1158/0008-5472.CAN-14-0155
5. Luo W, Wang J, Chen H, Ye L, Qiu J, Liu Y, et al. Epidemiology of pancreatic cancer: New version, new vision. Chin J Cancer Res. 2023;35(5):438-50. https://doi.org/10.21147/j.issn.1000-9604.2023.05.03
6. Stoffel EM, Brand RE, Goggins M. Pancreatic cancer: changing epidemiology and new approaches to risk assessment, early detection, and prevention. Gastroenterology. 2023;164(5):752-65. https://doi.org/10.1053/j.gastro.2023.02.012
7. Wang X, Liu C, Yang Y, Huang X, Yu J. Burden of pancreatic cancer in older adults globally, regionally, and in 204 countries: 1990-2019 and projections to 2030. J Gastrointest Surg. 2024;28(2):121-31. https://doi.org/10.1016/j.gassur.2023.12.001
8. Huber MA, Nadella S, Cao H, Kallakury B, Tucker RD, Gay MD, et al. Does chronic use of high dose proton pump inhibitors increase risk for pancreatic cancer? Pancreas. 2022;51(9):1118. https://doi.org/10.1097/MPA.0000000000002145
9. Singh P, Walker JP, Townsend CM, Thompson JC. Role of gastrin and gastrin receptors on the growth of a transplantable mouse colon carcinoma (MC-26) in BALB/C mice. Cancer Res. abril de 1986;46(4 Pt 1):1612-6.
10. Smith JP, Shih AH, Wotring MG, McLaughlin PJ, Zagon IS. Characterization of CCK-B/gastrin-like receptors in human gastric carcinoma. Int J Oncol. 1998;12(2):411-9.
11. Bergin E, Zylberberg HM, Lebwohl B, Freedberg DE. Trends in use of proton pump inhibitors among adults in the United States from 1999 to 2018. Pharmacoepidemiol Drug Saf. 2023;32(12):1406-10. https://doi.org/10.1002/pds.5676
12. Daniels B, Pearson SA, Buckley NA, Bruno C, Zoega H. Long-term use of proton-pump inhibitors: whole-of-population patterns in Australia 2013-2016. Ther Adv Gastroenterol. 2020;13:1756284820913743. Disponible en: https://doi.org/10.1177/1756284820913743
13. Muheim L, Signorell A, Markun S, Chmiel C, Neuner-Jehle S, Blozik E, et al. Potentially inappropriate proton-pump inhibitor prescription in the general population: a claims-based retrospective time trend analysis. Ther Adv Gastroenterol. 2021;14:1756284821998928. https://doi.org/10.1177/1756284821998928
14. Metz DC. Long-term use of proton-pump inhibitor therapy. Gastroenterol Hepatol 2008;4(5):322-5.
15. Castellana C, Pecere S, Furnari M, Telese A, Matteo MV, Haidry R, et al. Side effects of long-term use of proton pump inhibitors: practical considerations. Pol Arch Intern Med. 29 de junio de 2021;131(6):541-9. https://doi.org/10.20452/pamw.15997
16. Chinzon D, Domingues G, Tosetto N, Perrotti M. Safety of long-term proton pump inhibitors: facts and myths. Arq Gastroenterol. 2022;59(2):219-25. https://doi.org/10.1590/S0004-2803.202202000-40
17. da Maia TF, de Camargo BG, Pereira ME, de Oliveira CS, Guiloski IC. Increased risk of fractures and use of proton pump inhibitors in menopausal women: a systematic review and meta-analysis. Int J Environ Res Public Health. 2022;19(20):13501. https://doi.org/10.3390/ijerph192013501
18. Hutton B, Catalá-López F, Moher D. The prisma statement extension for systematic reviews incorporating network meta-analysis: prisma-nma. Med Clínica Engl Ed. 2016;147(6):262-6. https://doi.org/10.1016/j.medcli.2016.02.025
19. Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses. Eur J Epidemiol. 2010;25(9):603-5. HTTPS://DOI.ORG/10.1007/S10654-010-9491-Z
20. Shimonovich M, Pearce A, Thomson H, Keyes K, Katikireddi SV. Assessing causality in epidemiology: revisiting Bradford Hill to incorporate developments in causal thinking. Eur J Epidemiol. 2021;36(9):873-87. https://doi.org/10.1007/s10654-020-00703-7
21. Peng YC, Lin CL, Hsu WY, Lu IT, Yeh HZ, Chang CS, et al. Proton pump inhibitor use is associated with risk of pancreatic cancer: a nested case-control study. Dose-Response. 2018;16(4). https://doi.org/10.1177/1559325818803283
22. Hicks B, Friis S, Pottegárd A. Use of proton pump inhibitors and risk of pancreatic cancer. Pharmacoepidemiol Drug Saf. 2018;27(8):926-30. https://doi.org/10.1002/pds.4576
23. Lassalle M, Le Tri T, Afchain P, Camus M, Kirchgesner J, Zureik M, et al. Use of Proton pump inhibitors and risk of pancreatic cancer: a nationwide case-control study based on the French National Health Data System (snds). Cancer Epidemiol Biomarkers Prev. 2022;31(3):662-9. https://doi.org/10.1158/1055-9965.EPI-21-0786
24. Shih Wei L, Fung Chang S, Cheng Li L, Kuan Fu L. Use of proton pump inhibitors correlates with increased risk of pancreatic cancer: a case-control study in Taiwan. 2014. Kuwait Med. J. 2014;46(1):44-8.
25. Hwang IC, Chang J, Park SM. Association between proton pump inhibitor use and the risk of pancreatic cancer: A Korean nationwide cohort study. PLoS ONE. 2018;13(9):e0203918. https://doi.org/10.1371/journal.pone.0203918
26. Anandabaskar N. Pharmacoepidemiology. En: Raj GM, Raveendran R, editores. Introduction to basics of pharmacology and toxicology. Vol 1: General and molecular pharmacology: principles of drug action. Singapore: Springer; 2019. p. 271-80.
27. Lee JK, Merchant SA, Schneider JL, Jensen CD, Fireman BH, Quesenberry CP, et al. Proton pump inhibitor use and risk of gastric, colorectal, liver, and pancreatic cancers in a community-based population. Off J Am Coll Gastroenterol ACG. 2020;115(5):706. https://doi.org/10.14309/ajg.0000000000000591
28. Kearns MD, Boursi B, Yang YX. Proton pump inhibitors on pancreatic cancer risk and survival. Cancer Epidemiol. 2017;46:80-4. https://doi.org/10.1016/j.canep.2016.12.006
29. McCarthy DM. Proton pump inhibitor use, hypergastrinemia, and gastric carcinoids— what is the relationship? Int J Mol Sci. 2020;21(2):662. https://doi.org/10.3390/ijms21020662
30. Wang Y, Yang G, You L, Yang J, Feng M, Qiu J, et al. Role of the microbiome in occurrence, development and treatment of pancreatic cancer. Mol Cancer. 2019;18(1):173. https://doi.org/10.1186/s12943-019-1103-2
31. Sethi V, Vitiello GA, Saxena D, Miller G, Dudeja V. The Role of the microbiome in immunologic development and its implication for pancreatic cancer immunotherapy. Gastroenterology. 2019;156(7):2097-2115.e2. https://doi.org/10.1053/j.gastro.2018.12.045
32. Wei MY, Shi S, Liang C, Meng QC, Hua J, Zhang YY, et al. The microbiota and microbiome in pancreatic cancer: more influential than expected. Mol Cancer. 2019;18(1):97. https://doi.org/10.1186/s12943-019-1008-0
33. Banack HR, Bea JW, Kaufman JS, Stokes A, Kroenke CH, Stefanick ML, et al. The effects of reverse causality and selective attrition on the relationship between body mass index and mortality in postmenopausal women. Am J Epidemiol. 2019;188(10):1838-48. https://doi.org/10.1093/aje/kwz160
34. Savitz DA, Wellenius GA. Can cross-sectional studies contribute to causal inference? it depends. Am J Epidemiol. 2023;192(4):514-6. https://doi.org/10.1093/aje/kwac037
35. Yarmolinsky J, Wade KH, Richmond RC, Langdon RJ, Bull CJ, Tilling KM, et al. Causal inference in cancer epidemiology: what is the role of Mendelian randomization? Cancer Epidemiol Biomark Prev. 2018;27(9):995-1010. https://doi.org/10.1158/1055-9965.EPI-17-1177
36. Sugumar K, Gendi S, Quereshy HA, Gupta S, Hue JJ, Rothermel LD, et al. An analysis of time to treatment in patients with pancreatic adenocarcinoma. Surgery. 2023;174(1):83-90. https://doi.org/10.1016/j.surg.2023.03.011
37. Koltai T. Earlier diagnosis of pancreatic cancer: is it possible? Cancers. 2023;15(18):4430. https://doi.org/10.3390/cancers15184430
38. Kay K, Dolcy K, Bies R, Shah DK. Estimation of solid tumor doubling times from progression-free survival plots using a novel statistical approach. AAPS J. 2019;21(2):27. https://doi.org/10.1208/s12248-019-0302-5
39. Kwon D, Simon SL, Hoffman FO, Pfeiffer RM. Frequentist model averaging for analysis of dose-response in epidemiologic studies with complex exposure uncertainty. PLoS ONE. 2023;18(12):e0290498. https://doi.org/10.1371/journal.pone.0290498
40. Domínguez-Lara SA. El odds ratio y su interpretación como magnitud del efecto en investigación. Educ Médica. 2018;19(1):65-6. https://doi.org/10.1016/j.edumed.2017.01.008
41. Domínguez-Lara S. Magnitud del efecto, una guía rápida. Educ Médica. 2018;19(4):251-4. https://doi.org/10.1016/j.edumed.2017.07.002
42. Aguayo-Albasini JL, Flores-Pastor B, Soria-Aledo V. Sistema grade: clasificación de la calidad de la evidencia y graduación de la fuerza de la recomendación. Cir Esp. 2014;92(2):82-8. https://doi.org/10.1016/j.ciresp.2013.08.002
43. Nowinski CJ, Bureau SC, Buckland ME, Curtis MA, Daneshvar DH, Faull RLM, et al. Applying the Bradford Hill criteria for causation to repetitive head impacts and chronic traumatic encephalopathy. Front Neurol. 2022;13. https://doi.org/10.3389/fneur.2022.938163
44. Raj AT, Sujatha G, Muruganandhan J, Kumar SS, Bharkavi SI, Varadarajan S, et al. Reviewing the oral carcinogenic potential of E-cigarettes using the Bradford Hill criteria of causation. Transl Cancer Res. 2020;9(4):3142-52. https://doi.org/10.21037/tcr.2020.01.23
45. VanderWeele TJ. Principles of confounder selection. Eur J Epidemiol. 2019;34(3):211-9. https://doi.org/10.1007/s10654-019-00494-6
46. Zeraatkar D, Cheung K, Milio K, Zworth M, Gupta A, Bhasin A, et al. Methods for the selection of covariates in nutritional epidemiology studies: a meta-epidemiological review. Curr Dev Nutr. 2019;3(10):98-104. https://doi.org/10.1093/cdn/nzz104
47. Conroy T, Pfeiffer P, Vilgrain V, Lamarca A, Seufferlein T, O'Reilly EM, et al. Pancreatic cancer: esmo clinical practice guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023;34(11):987-1002. https://doi.org/10.1016/j.annonc.2023.08.009
48. Sohal DPS, Kennedy EB, Khorana A, Copur MS, Crane CH, Garrido-Laguna I, et al. Metastatic pancreatic cancer: asco clinical practice guideline update. J Clin Oncol. 2018;36(24):2545-56. https://doi.org/10.1200/JCO.2018.78.9636
49. Principe DR, Rana A. Updated risk factors to inform early pancreatic cancer screening and identify high risk patients. Cancer Lett. 2020;485:56-65. https://doi.org/10.1016/j.canlet.2020.04.022
50. Tempero MA, Malafa MP, Al-Hawary M, Behrman SW, Benson AB, Cardin DB, et al. Pancreatic adenocarcinoma, version 2.2021, nccn clinical practice guidelines in oncology. J Natl Compr Canc Netw. 2021;19(4):439-57. https://doi.org/10.6004/jnccn.2021.0017
51. Zhao Z, Liu W. Pancreatic cancer: a review of risk factors, diagnosis, and treatment. Technol Cancer Res Treat. 2020;19:1533033820962117. https://doi.org/10.1177/1533033820962117
52. Gheorghe G, Diaconu CC, Ionescu V, Constantinescu G, Bacalbasa N, Bungau S, et al. Risk factors for pancreatic cancer: emerging role of viral hepatitis. J Pers Med. 2022;12(1):83. https://doi.org/10.3390/jpm12010083
53. Arafa A, Eshak ES, Abdel Rahman TA, Anwar MM. Hepatitis C virus infection and risk of pancreatic cancer: a meta-analysis. Cancer Epidemiol. 2020;65:101691. https://doi.org/10.1016/j.canep.2020.101691
54. Song C, Lv J, Liu Y, Chen JG, Ge Z, Zhu J, et al. Associations between hepatitis B virus infection and risk of all cancer types. Jama Netw Open. 2019;2(6):e195718. https://doi.org/10.1001/jamanetworkopen.2019.5718
55. Xiang X, Chen X, Ye S, Wang S, Xiao Y, Wang X, et al. Pancreatic cancer challenge in 52 Asian countries: age-centric insights and the role of modifiable risk factors (1990-2019). Front Oncol. 2023;13. https://doi.org/10.3389/fonc.2023.1271370
56. Gad MM, Gãman MA, Saad AM, Al-Husseini MJ, Shehata OA, Saleh MA, et al. Temporal trends of incidence and mortality in Asian-Americans with pancreatic adenocarcinoma: an epidemiological study. Ann Gastroenterol. 2020;33(2):210-8. https://doi.org/10.20524/ aog.2020.0450
57. Yin L, Wei J, Lu Z, Huang S, Gao H, Chen J, et al. Prevalence of germline sequence variations among patients with pancreatic cancer in China. Jama Netw Open. 2022;5(2):e2148721. HTTPS://DOI.ORG/10.1001/JAMANETWORKOPEN.2021.48721
58. Lima JJ, Thomas CD, Barbarino J, Desta Z, Van Driest SL, El Rouby N, et al. Clinical pharmacogenetics implementation consortium (CPIC) guideline for CYP2C19 and proton pump inhibitor dosing. Clin Pharmacol Ther. 2021;109(6):1417-23. https://doi.org/10.1002/cpt.2015
59. Alvarado ÁT, Muñoz AM, Loja B, Miyasato JM, García JA, Cerro RA, et al. Estudio de las variantes alélicas cyp2c9*2 y CYP2C9*3 en muestras de población mestiza peruana. Biomédica. 2019;39(3):601-10. https://doi.org/10.7705/biomedica.4636