10.12804/revistas.urosario.edu.co/revsalud/a.14383
PRESENTACIÓN DE CASO
Tonatiuh González Heredia 1
Marlene Stephanie González Francisco 2
María Fernanda Sánchez Gutiérrez 3
Juan Carlos Gutiérrez Delgado 4
Héctor Josué Medina Andrade 5
1 Departamento de Ciencias Biomédicas, Centro Universitario de Tonalá, Universidad de Guadalajara (México).
 0000-0003-4089-5462
0000-0003-4089-5462
 tonatiuh.gonzalez2923@academicos.udg.mx
tonatiuh.gonzalez2923@academicos.udg.mx
2 Centro Médico Nacional de Occidente, Instituto Mexicano del Seguro Social (México).
 0009-0007-4845-4617
0009-0007-4845-4617
3 Departamento de Ciencias Biomédicas, Centro Universitario de Tonalá, Universidad de Guadalajara (México).
 0009-0009-2900-0534
0009-0009-2900-0534
4 Departamento de Ciencias Biomédicas, Centro Universitario de Tonalá, Universidad de Guadalajara (México).
 0009-0002-1020-2485
0009-0002-1020-2485
5 Centro Médico Nacional de Occidente, Instituto Mexicano del Seguro Social (México).
 0000-0002-0493-0315
0000-0002-0493-0315
Recibido: 24 de septiembre de 2024
Aprobado: 11 de diciembre de 2024
Recibido: 24 de septiembre de 2024
Aprobado: 11 de diciembre de 2024
Para citar este artículo: González Heredia T, Gonzalez Francisco MS, Sánchez Gutiérrez MF, Gutiérrez Delgado JC, Medina Andrade HJ. Diagnóstico de tumor óseo primario de células gigantes en la columna torácica: presentación de caso y hallazgos de imagen. Rev Cienc Salud. 2025;23(1):1-12. https://doi.org/10.12804/revistas.urosario.edu.co/revsalud/a.14383
Resumen
Introducción: el tumor óseo células gigantes (TCG) se ha descrito como una
neoplasia localmente agresiva con metástasis infrecuente. Está compuesto por un estroma mononuclear, macrófagos y células
gigantes similares a los osteoclastos. Suele aparecer entre los 20 y los 40 años de edad tanto en
hombres como en mujeres. Su localización más frecuente son los huesos
proximales a la rodilla, dentro de los cuales el fémur distal y la tibia proximal son los más afectados.
Los sitios menos frecuentes son el radio, en su porción distal, el fémur proximal, el pie y la región pélvica. Es raro que este tumor
involucre el esqueleto axial, tanto que en la literatura solo
se han descrito dos: los de región sacra, con una frecuencia del 5 %-15 % de los casos.
Presentación del caso: correspondió a un
hombre con TCG de presentación
clínica atípica, con localización
primaria en la columna torácica y la extensión extraósea extensa, por
infiltración al pulmón y al foramen vertebral.
Discusión: las
características clínicas clásicamente asociadas con el TCG se relacionan con su localización anatómica; sin
embargo, en este caso, al estar ubicado en la columna torácica con invasión al
mediastino y el pulmón, dieron lugar a la presentación clínica inicial atípica en el paciente. En
este tipo de casos que suponen un reto diagnóstico, los hallazgos
imagenológicos desempeñan un papel crucial para orientar el abordaje médico,
mientras que el estudio histopatológico es determinante.
Palabras clave: tumor de células gigantes; neoplasia ósea; neoplasia de tejido óseo; diagnóstico imagenológico.
Abstract
Introduction: Giant cell bone tumor (GCT) is a locally aggressive neoplasm
with rare metastasis. It is composed of mononuclear stroma, macrophages and
osteoclast-like giant cells. It classically occurs between the ages of 20 and
40 in both men and women. Its most frequent location is the bones proximal to
the knee, with the distal femur and proximal tibia being the most affected.
Other less common sites are the distal radius, proximal femur, foot and pelvic
region. Presentations involving the axial skeleton are rare, with only those in
the sacral region described in the literature with a frequency of 5-15% of
cases.
Case presentation: Below
is the clinical case of a male with GCT with
atypical clinical presentation with primary location in the thoracic spine and
extensive extraosseous extension due to infiltration to the lung and vertebral
foramen.
Discussion: The clinical
characteristics that are classically associated with giant cell bone tumors are
related to their anatomical location. However, in the case presented, the
atypical primary location in the thoracic spine with invasion to the
mediastinum and lung gave rise to the patient's initial atypical clinical
presentation. In these types of cases that pose a diagnostic challenge, imaging
findings play a crucial role in guiding the medical approach, while the
histopathological study is decisive.
Keywords: giant cell tumors; giant cell tumor of bone; neoplasms, bone tissue; diagnostic imaging.
Resumo
Introdução: o tumor ósseo de células gigantes (TOCG) é descrito como uma neoplasia localmente agressiva com metástase infrequente e é
composta de estroma mononuclear, macrófagos e células gigantes semelhantes a osteoclastos. Geralmente ocorre entre 20 e 40 anos de idade, tanto em homens quanto em mulheres. Os
locais mais comuns são os ossos próximos ao joelho, sendo o fêmur distal e a tíbia proximal os mais comumente afetados.
Outros locais menos frequentes são o rádio distal, o fêmur proximal, o pé e a região pélvica. As
apresentações que envolvem o esqueleto axial são raras, sendo que apenas
aquelas na região sacral são descritas na literatura com uma frequência de 5 a
15% dos casos.
Apresentação do caso: o caso
clínico a seguir é de um TOCG do
sexo masculino com apresentação clínica atípica, com localização primária na
coluna torácica e grande extensão extraóssea por
infiltração do pulmão e do forame vertebral.
Discussão: as características clínicas
classicamente associadas aos TOCGS estão
relacionadas à sua localização anatómica. No entanto, no caso apresentado, a
localização primária atípica na coluna torácica com invasão do mediastino e do
pulmão deu origem à apresentação clínica inicial atípica do paciente. Nesses
casos de diagnóstico desafiador, os achados de imagem desempenham papel crucial
na orientação da abordagem médica, enquanto o estudo histopatológico é
decisivo.
Palavras-chave: tumor de células gigantes; neoplasia óssea; neoplasia de tecido ósseo; diagnóstico por imagem.
Introducción
En la Clasificación de Tumores de Tejido Blando y Hueso del 2020 de la Organización Mundial de la Salud, se describió el tumor óseo células gigantes (TOCG) como una neoplasia localmente agresiva con metástasis infrecuente. En el plano histológico, está compuesto por un estroma mononuclear, macrófagos y células gigantes similares a los osteoclastos (1). Suele aparecer entre los 20 y los 40 años de edad con un pico de incidencia en la tercera década de la vida, tanto en hombres como en mujeres (2,3).
Su localización más frecuente son los huesos proximales a la rodilla, dentro de los cuales el fémur distal y la tibia proximal son los más afectados. Otros sitios menos frecuentes son el radio en su porción distal, el fémur proximal, el pie y la región pélvica (4). La evidencia sobre casos que involucran el esqueleto axial es muy limitada; algunos autores la citan entre el 2 % y el 15 °/o, con predominio por la región sacra (5,6).
Pese a su limitada capacidad de metástasis, algunos estudios han indicado que se disemina al pulmón en el 3.5 % al 5 % de los casos. Así mismo, se reporta una incidencia de malignidad del 4 % (7-9).
A continuación, el caso clínico de un hombre con TOCG de presentación clínica atípica con localización primaria en la columna torácica y extensión extraósea extensa por infiltración al pulmón y al foramen vertebral.
Presentación del caso
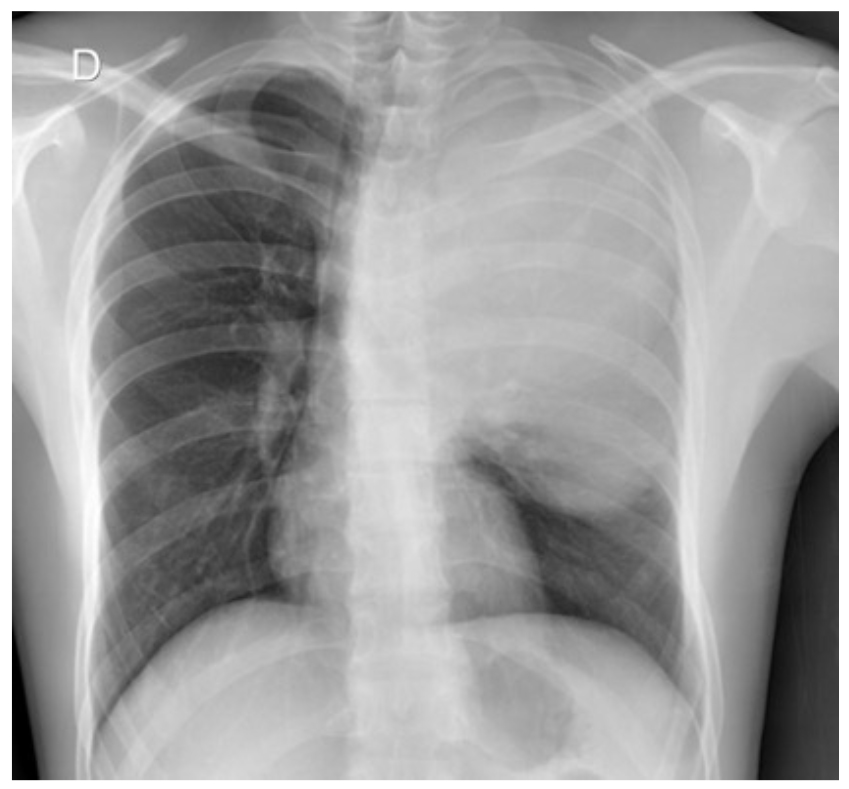
El caso corresponde a un hombre de 38 años de edad, sin antecedentes de importancia, cuyo padecimiento inició dos meses antes, con astenia, adinamia y fatiga, que dificultaba actividades de la vida cotidiana, además de tos seca y disnea de grandes esfuerzos. Acudió a atención médica y se le indicó tratamiento sintomático, pero no hubo mejoría. Diez días después, tuvo tos en accesos y la disnea se fue incrementando progresivamente hasta incluso aparecer en reposo. Se le indicó manejo sintomático, pero tampoco mejoró el cuadro clínico. Se le solicitó, entonces una radiografía de tórax, en la cual se observó una lesión pulmonar ocupativa en lóbulo superior izquierdo (figura 1).
Figura 1. Radiografía posteroanterior de tórax que muestra una lesión pulmonar en el lóbulo superior izquierdo, radiopaca, con aspecto sólido, bordes bien definidos, con efecto masa sobre la tráquea, bronquios y grandes vasos que se desplazan en sentido contralateral, con un tamaño aproximado de 16 x 10 cm en sus ejes longitudinal y transverso
El abordaje continuó con el servicio de oncología médica. En la exploración física en el tórax se encontró con amplexión y amplexación disminuida y murmullo vesicular disminuido en el hemitórax izquierdo, mate a la percusión, ruidos cardiacos rítmicos, de buena intensidad. El resto de hallazgos no son relevantes al caso.
Después de ello se le tomó al paciente una tomografía contrastada que, en el plano axial, en el hemitórax izquierdo, mostró una tumoración que involucraba los segmentos apicoposterior y anterior del lóbulo superior y el segmento apical del lóbulo inferior. Medía aproximadamente 10.9 cm x 12.3 cm x 14.4 cm en sentido latero-lateral, anteroposterior y cefalocaudal, con densidad heterogénea (figura 2). Se observaron áreas sólidas que realzaban tras la administración de medio de contraste intravenoso, con zonas de necrosis de predominio en la mitad inferior. Los bordes eran lobulados e infiltraba la grasa mediastinal. En el corte coronal, se visualizó un efecto masa que desplazaba la tráquea, la carina y los bronquios, en sentido contralateral (figuras 3A y 3B).
Figura 2. Tomografía contrastada, corte axial de hemitórax
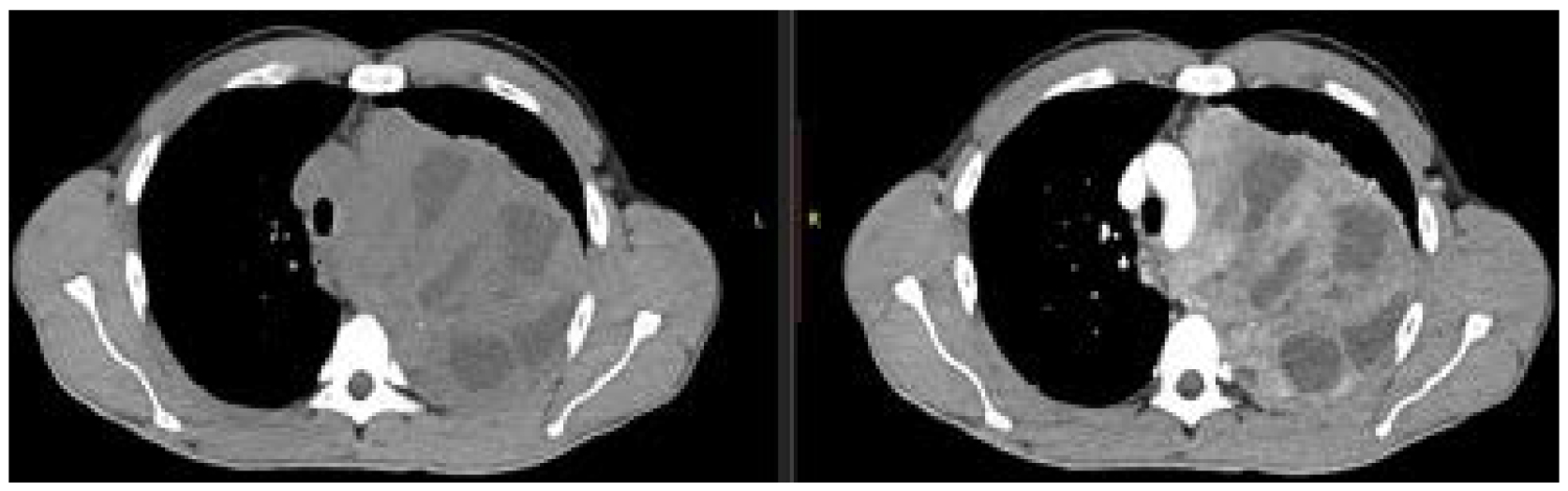
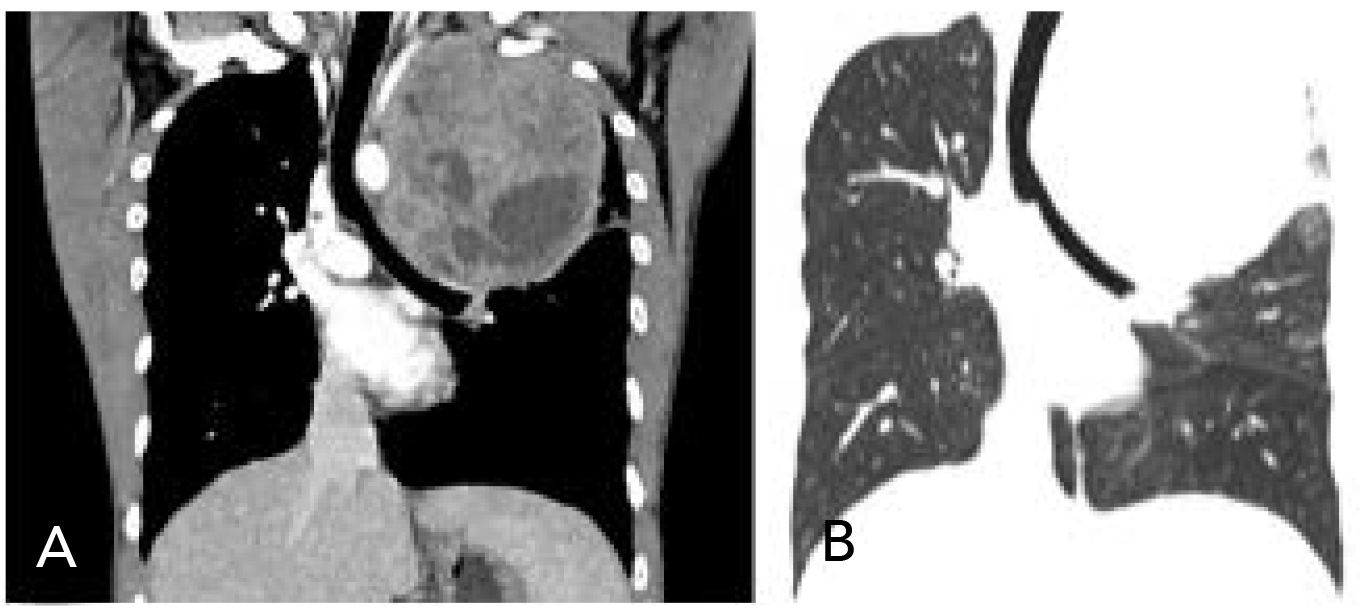
Figura 3. Tomografía contrastada, en reconstrucción coronal. A) Masa heterogénea en el pulmón izquierdo que desplaza la tráquea en sentido contralateral. B) Ventana pulmonar
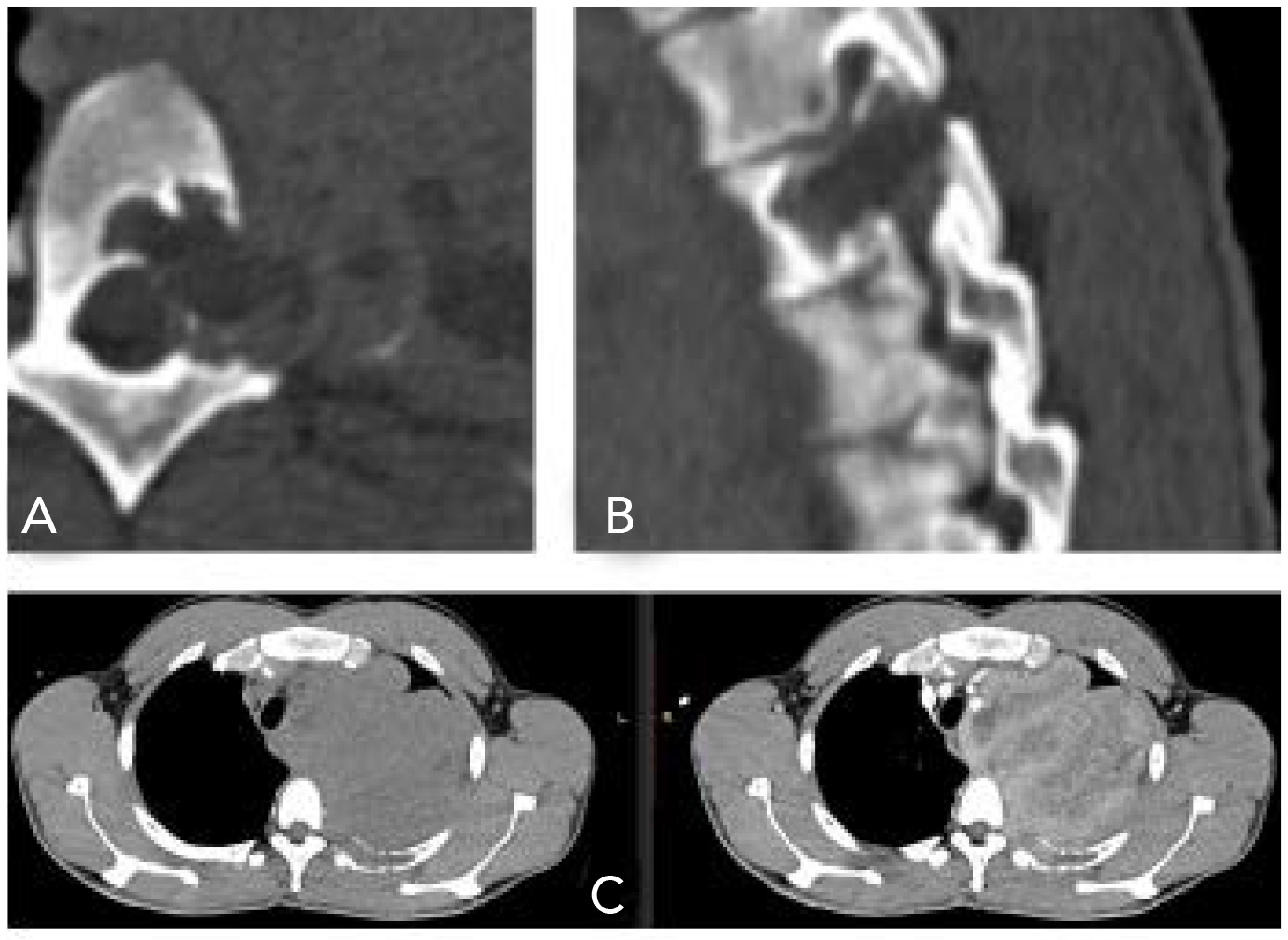
En el corte axial y sagital se observó una lesión ósea lítica, con bordes geográficos que afectaban el pedículo, parte del cuerpo y de la apófisis transversa de la vértebra T4, así como la parte posterior del cuarto arco costal izquierdo. Dicha lesión se extendía en sentido caudal y se introducía al foramen de T3-T4 y T4-T5 (figuras 4A y 4B). Al hacer contacto con la duramadre, condicionaba el desplazamiento de la arteria y la vena subclavias, pero no las comprimía.
Figura 4. A) Corte axial a la altura de T4. B) Corte sagital T3-T5. C) Reconstrucción de corte transversal a la altura de T3
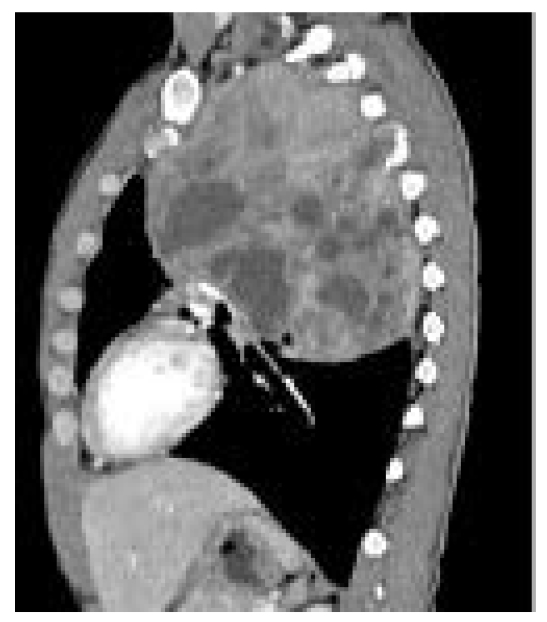
En el lóbulo inferior se notaron 6 pequeños nódulos de aspecto sólido. Así mismo, el hemitórax derecho evidenciaba 3 nódulos subpleurales menores de 6 mm, al igual que adenopatías de aspecto atípico en el nivel ganglionar intravenoso izquierdo del cuello y en el mediastino (figura 5).
Figura 5. Tomografía contrastada, reconstrucción sagital
Dos meses después, se le realizó una biopsia mediante aguja gruesa (TRU-CUT) de la lesión pulmonar. El informe indicó neoplasia de alta celularidad que constaba de células estromales tipo monocito con citoplasma eosinofílico moderado, células gigantes similares a osteoclastos, con 40 a 60 núcleos por célula (figura 6). No se encontró atipia, pleomorfismo, mitosis o necrosis. De la misma manera, no se encontraron células coincidentes con parénquima pulmonar o bronquial. En cuanto a la inmunohistoquímica, fue CD68 positivo en el citoplasma de las células gigantes multinucleadas (figura 7); el factor de transcripción de microftalmia fue positivo en los núcleos de las células gigantes multinucleadas (figura 8); el lisozima fue positivo y focal (figura 9). El Ki-67 estuvo al 20 %. La proteína S100 fue negativa. Todo lo anterior fue compatible con TCG.
Figura 6. Fragmentos TRU-CUT referidos como biopsia pulmonar, en la que se observa una neoplasia de alta celularidad compuesta por células estromales tipo monocito de citoplasma eosinófilo moderado, núcleo ovoide basófilo con nucleolo discreto y por células gigantes tipo osteoclasto en las que se cuentan de 40 a 60 núcleos por célula. Sin evidencia de parénquima pulmonar residual ni mucosa bronquial. Sin evidencia de mitosis, atipia o necrosis
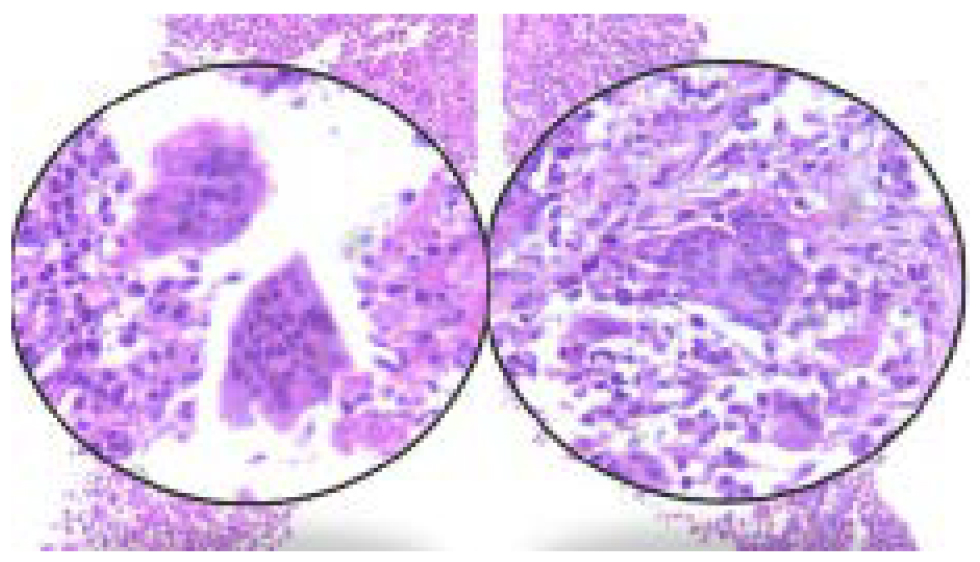
Figura 7. CD68: positivo en el citoplasma de las células gigantes multinucleadas
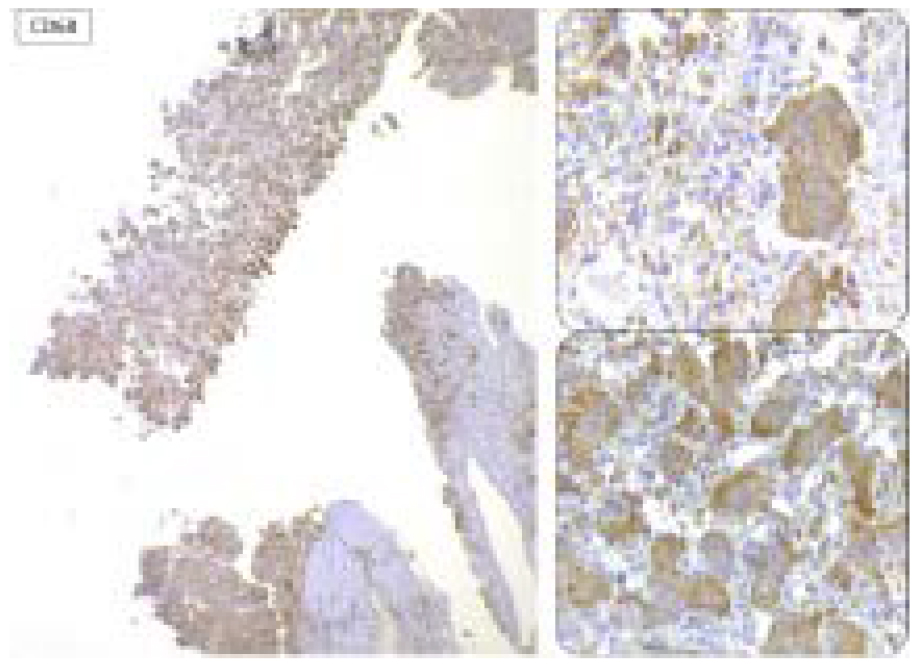
Figura 8. Factor de transcripción de microftalmia (MiTF): positivo en los núcleos de las células gigantes multinucleadas
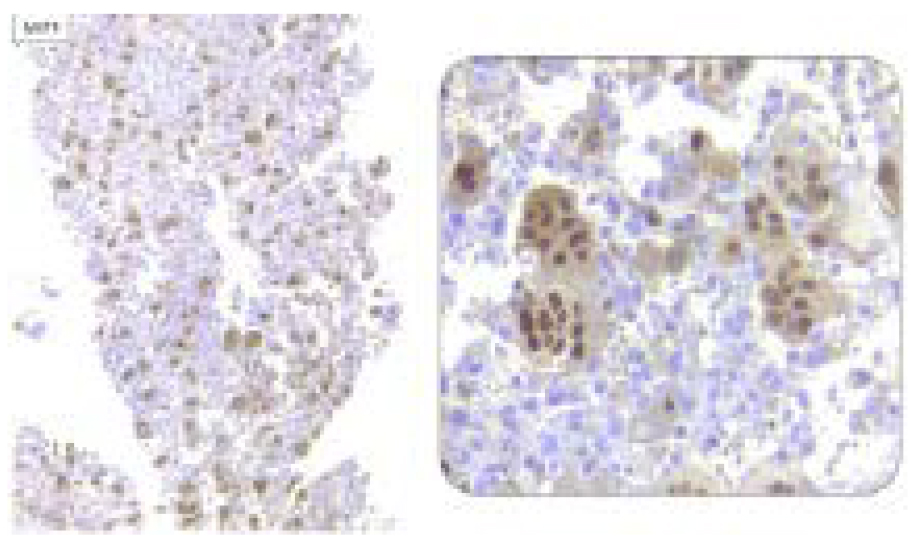
Figura 9. Lisozima: positivo focal en el citoplasma de las células gigantes multinucleadas y de las células estromales
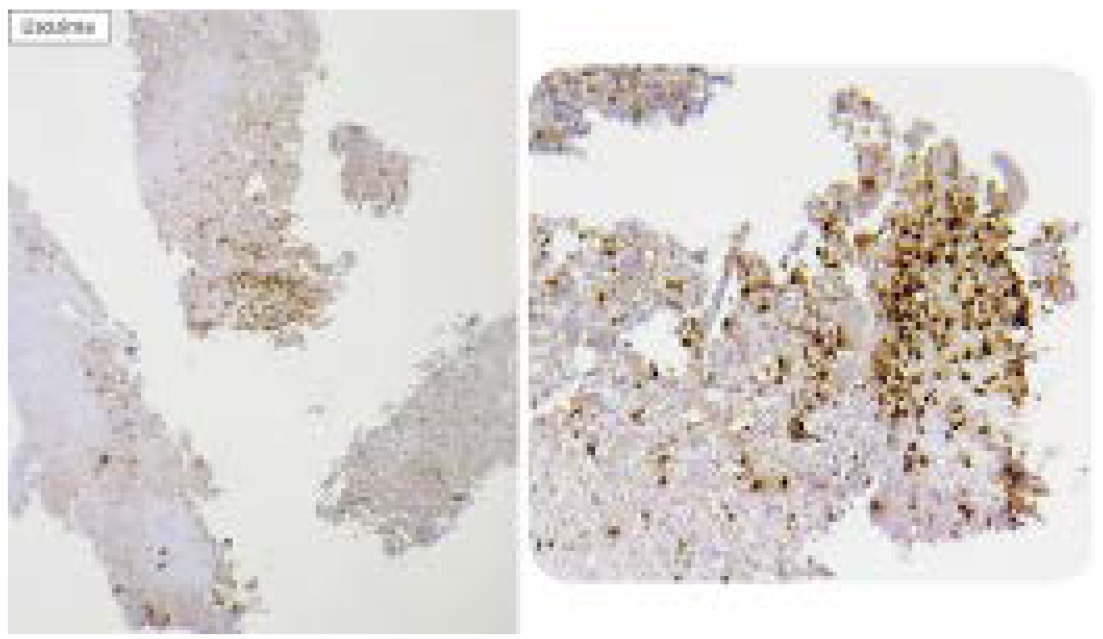
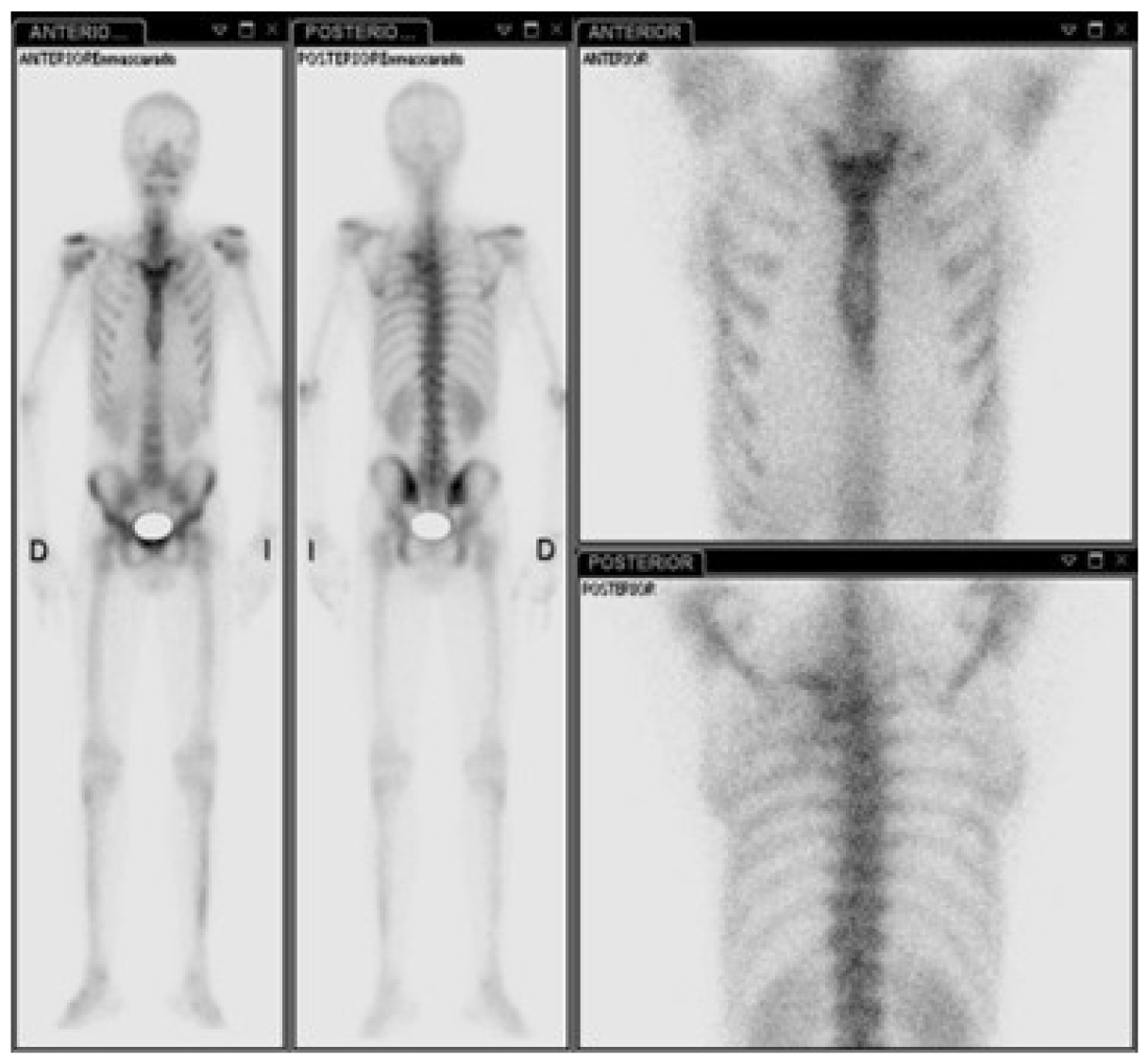
Para completar el abordaje, se le realizó al paciente una gammagrafía ósea que evidenció un tumor dependiente de vértebras torácicas que infiltraba el pulmón izquierdo y se introducía en el foramen vertebral de D3-D4, D4-D5, además de metástasis en los arcos costales cuarto y quinto izquierdos (figura 10).
Figura 10. Gammagrafía ósea vértebras D3-D4, D4-D5 con infiltración en pulmón izquierdo y arcos costales 4to y 5to izquierdos.
Según los hallazgos anteriores, al hombre se le diagnosticó TCG primario en la columna torácica con extensión extraósea extensa, por infiltración al pulmón y al foramen vertebral D3-D4, D4-D5.
El paciente se estadificó como enfermedad irresecable, por lo que se le recetó denosumab, con dosis de carga: 120 mg en los días 1, 8 y 15, y posterior mantenimiento con 120 mg, vía subcutánea, cada 28 días. Dicho tratamiento se le ofreció con el objetivo de controlar la enfermedad localmente, así como los síntomas.
Discusión
La presentación clínica típica de los pacientes con un TCG es dolor e hinchazón en la zona afectada, así como alteración de la marcha. Ello se asocia directamente con su localización más frecuente: el fémur distal y la tibia proximal (9). En el caso presentado, el paciente presentó una localización primaria atípica en la columna torácica con invasión al mediastino y el pulmón. Al ser una neoplasia localmente agresiva con limitada capacidad de metástasis, no quedó claro si los síntomas de tos, disnea y fatiga fueron condicionados por la invasión y compresión mecánica que ocasionaba el tumor o por la invasión de células neoplásicas en el parénquima pulmonar. A pesar de estas posibles explicaciones, se resalta que el paciente no se quejaba de dolor, hinchazón o de alguna otra molestia clínicamente relevante.
Los estudios de imagen, junto con la historia clínica y la exploración física, forman parte del estudio del paciente con dificultad respiratoria, disnea y tos, pues los hallazgos radiográficos pueden orientar la etiología del padecimiento.
Radiografía
La primera forma de imagen que se debe obtener es la radiografía simple. El TOCG de la columna vertebral puede mostrar una apariencia típica de "burbuja de jabón" o como una lesión puramente lítica. La naturaleza agresiva del tumor puede conducir a diversos grados de compresión vertebral, que va desde un colapso leve a una vértebra plana completa (6). Los pedículos ovalados del arco vertebral pueden aparecer deformados o desaparecer por destrucción. Los bordes de las áreas líticas son parcial o mal definidos, que se pierden con la masa de tejido blando asociada, como ocurre en el caso presentado, donde la masa no permite definir áreas líticas. No obstante, resaltan signos de compresión en el tejido adyacente, como la tráquea, el parénquima y los grandes vasos.
Su expansión en el tejido blando circundante se puede caracterizar como una sombra radiopaca. Dichas masas de tejidos blandos suelen aparecer sobre la línea paravertebral de la columna torácica, el músculo psoas y el tejido blando paravertebral anterior de la columna cervical (10).
Sobre la base de los hallazgos de la radiografía simple, las lesiones se clasifican según el sistema de Campanacci. Las lesiones de grado I están contenidas dentro del hueso. Las lesiones que tienen expansión de la corteza, pero no perforación, se clasifican como grado II, y las lesiones con perforación de la corteza y extensión a tejidos blandos se clasifican como grado III (8,11). Para el caso, debido a que no quedó claro el origen de la masa, la clasificación de Campanacci no fue aplicable con los hallazgos radiográficos.
Tomografía
Las modalidades de imágenes adicionales, como una tomografía computarizada, pueden ser útiles para identificar el grado de afectación de la corteza; además, ayuda en la toma de decisiones quirúrgicas. La tomografía computarizada también puede mostrar la formación de hueso dentro de la lesión, lo que sería una indicación de un osteosarcoma rico en células gigantes, en lugar de un TOCG (8).
En la tomografía computarizada, el tumor tiene atenuación de los tejidos blandos sin evidencia de matriz mineralizada. Las áreas de hemorragia o necrosis pueden crear una densidad heterogénea con focos de baja atenuación. Se identificó un borde esclerótico, tanto en el corte axial como en el sagital. Un margen esclerótico en la periferia del tumor no es infrecuente; se observa en el 33 % de los casos. Si la lesión se distribuye excéntricamente, el borde esclerótico delgado suele aparecer en el borde opuesto al lado excéntrico. Esta apariencia paradójica es útil para diagnosticar el TOCG (12).
La apariencia de "pompa de jabón" observada en la radiografía simple es secundaria a la seudotrabeculación, que se puede apreciar en cortes axiales de la tomografía. Se pueden ver algunos tabiques óseos que surgen del borde de la lesión y que se extienden hacia el interior de la masa. Los tabiques óseos cortos aparecen como estrías, y los tabiques más largos, como espolones (6). No obstante, en este caso no fueron observables trabeculaciones en la masa ósea.
Gammagrafía ósea
El TOCG produce una mayor absorción de radiofármacos como tecnio-99m. El patrón de aumento de la captación puede ser difuso (40 %) o periférico, con poca actividad central (60 %). Los patrones extendidos de captación de radiactividad, más allá de los márgenes del tumor, impiden una definición precisa de la extensión intramedular. Puede ocurrir un aumento de la captación en el hueso a través de la articulación adyacente y en otras articulaciones de la misma extremidad no afectadas por el tumor. Por lo tanto, el papel de la gammagrafía ósea en la TOCG es limitado, porque es inespecífico y poco fiable para definir la extensión del tumor. Sin embargo, es útil para evaluar al paciente raro con TOCG multicéntrico o metastásico (13).
El diagnóstico de TOCG es histológico. Se encuentra compuesto por células estromales mononucleares neoplásicas entremezcladas con células no mononucleares no neoplásicas y células gigantes multinucleadas tipo osteoclasto (10). Los osteoclastos provienen de la línea de monoci-macrófago y, al igual que estos, se ha documentado la expresión de CD68 en las células multinucleadas del TOCG (14).
El factor de transcripción asociado con microftalmia se usa como un indicador de diferenciación melanocítica; sin embargo, se ha descrito su presencia en distintos procesos tumorales, como el carcinoma renal, neoplasia perivascular de células epitelioides, sarcoma alveolar de partes blandas, hemangioendotelioma epitelioide, tumor fibromixoide y de células claras. Al igual que la CD68, es expresada por macrófagos y por osteoclastos, que se han hallado positivos en los procesos neoplásicos que involucran células gigantes osteoclásticas (9,15).
La proteína S100 se ha relacionado con la familia de neoplasias deficiente en smarcb1, y en casos menos frecuentes con tumores lipomatosos o sarcoma sinonasal; pero no es coincidente con el TOCG (10).
Conclusiones
La presentación primaria de un TOCG en la columna vertebral es una entidad infrecuente, cuyo abordaje es complementado mediante estudios de imagen. El conocer las características de los hallazgos imagenológicos le permiten al clínico un abordaje óptimo, ya que orientan tanto el diagnóstico como el enfoque terapéutico. Cabe resaltar que, pese a la correlación entre los estudios radiológicos y la entidad patológica, el diagnóstico final se debe efectuar no solo por métodos clínicos y radiológicos, sino apoyarse en estudios histológicos, que son la base para decidir la conducta quirúrgica y evitar recidivas que pueden progresar hasta convertirse en neoplasias que dejen secuelas permanentes en los pacientes.
Contribución de los autores
Conceptualización: Tonatiuh González Heredia y María Fernanda Sánchez Gutiérrez; metodología: María Fernanda Sánchez Gutiérrez; software: María Fernanda Sánchez Gutiérrez; investigación: Marlene Stephanie González Francisco, Juan Carlos Gutiérrez Delgado y Héctor Josué Medina Andrade; redacción y preparación del borrador original: Tonatiuh González Heredia y María Fernanda Sánchez Gutiérrez; revisión y edición: Tonatiuh González Heredia y María Fernanda Sánchez Gutiérrez. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Conflicto de intereses
Los autores involucrados en esta investigación declaran no presentar conflicto de intereses.
Referencias
1. Cao H, Lin F, Hu Y, Zhao L, Yu X, Wang Z, et al. Epidemiological and clinical features of primary giant cell tumors of the distal radium: a multicenter retrospective study in China. Sci Rep. 2017 Aug 22;7(1):9067. https://doi.org/10.1038/s41598-017-09486-6
2. Choi JH, Ro JY. The 2020 who classification of tumors of bone: an updated review. Adv Anat Pathol. 2021 May 1;28(3):119-38. https://doi.org/10.1097/PAP.0000000000000293
3. Deventer N, Budny T, Gosheger G, Rachbauer A, Puetzler J, Theil JC, et al. Giant cell tumor of bone: a single center study of 115 cases. J Bone Oncol. 2022 Feb 17;33:100417. HTTPS://DOI.ORG/10.1016/J.JBO.2022.100417
4. Hashimoto K, Nishimura S, Miyamoto H, Toriumi K, Ikeda T, Akagi M. Comprehensive treatment outcomes of giant cell tumor of the spine: a retrospective study. Medicine (Baltimore). 2022 Aug 12;101(32):e29963. https://doi.org/10.1097/MD.0000000000029963
5. Konishi E, Outani H, Mano M, Nagata S, Shirai T, Naka N, et al. Giant cell tumor of bone: analysis of 213 cases involving extra-craniofacial bones. Pathol Int. 2021 Aug;71(8):500-511. https://doi.org/10.1111/pin.13107
6. Leggett AR, Berg AR, Hullinger H, Benevenia JB. Diagnosis and treatment of lumbar giant cell tumor of the spine: update on current management strategies. Diagnostics (Basel). 2022 Mar 30;12(4):857. https://doi.org/10.3390/diagnostics12040857
7. Liu X, Lou C, Huang Z. Giant cell tumor of lumbar vertebrae on MR and 18F-fdg pet/CT: a case report and literature review. J Belg Soc Radiol. 2023 Mar 6;107(1):17. https://doi.org/10.5334/jbsr.3012
8. Basu Mallick A, Chawla SP. Giant cell tumor of bone: an update. Curr Oncol Rep. 2021 Mar 22;23(5):51. https://doi.org/10.1007/s11912-021-01047-5
9. Mohanty SK, Sharma S, Pradhan D, Kandukuri SR, Farahani N, Barry C, et al. Microphthalmia-associated transcription factor (MiTF): promiscuous staining patterns in fibrohistiocytic lesions is a potential pitfall. Pathol Res Pract. 2018 Jun;214(6):821-5. HTTPS://DOI.ORG/10.1016/J.PRP.2018.05.001
10. Schaefer IM, Hornick JL. Diagnostic immunohistochemistry for soft tissue and bone tumors: an update. Adv Anat Pathol. 2018 Nov;25(6):400-2. https://doi.org/10.1097/PAP.0000000000000204
11. Palmerini E, Picci P, Reichardt P, Downey G. Malignancy in giant cell tumor of bone: a review of the literature. Technol Cancer Res Treat. 2019 Jan 1;18:1533033819840000. https://doi.org/10.1177/1533033819840000
12. Shi LS, Li YQ, Wu WJ, Zhang ZK, Gao F, Latif M. Imaging appearance of giant cell tumour of the spine above the sacrum. Br J Radiol. 2015 Jul;88(1051):20140566. https://doi.org/10.1259/bjr.20140566
13. Montgomery C, Couch C, Emory CL, Nicholas R. Giant cell tumor of bone: review of current literature, evaluation, and treatment options. J Knee Surg. 2019 Apr;32(4):331-336. https://doi.org/10.1055/s-0038-1675815.
14. Shibuya I, Miki T, Kawamoto M, Karakawa A, Nakamura S, Kamijo R. Immunohistochemical analysis of the distribution of RANKL-expressing cells and the expression of osteoclast-related markers in giant cell tumor of bone. J Hard Tissue Biol. 2020;29(3):137-46. https://doi.org/10.2485/jhtb.29.137.
15. Wei S, Testa JR, Argani P. A review of neoplasms with MITF/MíT family translocations. Histol Histopathol. 2022 Apr;37(4):311-321. https://doi.org/10.14670/HH-18-426