Introducción
La anticoagulación es la piedra angular en el tratamiento de diferentes enfermedades, como son la prevención de accidente cerebrovascular, la fibrilación auricular y la enfermedad tromboembólica venosa. En el mundo, el número de pacientes anticoagulados viene en aumento y, por lo tanto, también los efectos adversos relacionados con ello. En un estudio llevado a cabo en Estados Unidos, los anticoagulantes estuvieron implicados en aproximadamente el 14.9 % del total de visitas a urgencias, por efectos adversos de medicamentos, más que con cualquier otra clase de medicamentos 1. El principal efecto adverso de la anticoagulación es el sangrado. Las tasas estimadas de sangrado con warfarina son muy variables. Algunos estudios reportan tasas del 0.6 % anual de sangrado fatal, 3.0 % de sangrado mayor y 9.6 % para cualquier sangrado 2. Con los anticoagulantes orales de acción directa (ACOD) se han informado tasas menores de sangrado mayor, específicamente de hemorragia intracraneana 3,4. Los sitios más comunes de sangrado son el tubo digestivo, los tejidos blandos y las vías urinarias 2.
El hematoma espontáneo de pared abdominal (HEPA) es uno de los sitios menos frecuentes y, por ende, menos estudiados. La incidencia reportada es variable por diversas series de casos y se describe la anticoagulación como el principal factor de riesgo 5,6. En una cohorte retrospectiva en Estados Unidos se identificó que el 77.4 % de los pacientes estaba en manejo anticoagulante, el 58.5 % tenía enfermedad renal crónica, el 51.3 % recibía inyecciones abdominales; el 33.9 % tenía tos y el 29.5 % estaba en terapia antiplaquetaria 7.
Cualquier condición que aumente de forma transitoria y súbita la presión intrabdominal, como el vómito o la tos, puede asociarse con HEPA. Son pocos los casos reportados en la literatura en los que el anticoagulante asociado era un ACOD, y en todos estos casos se identificó un factor de riesgo adicional a la anticoagulación. La mayoría de los casos responde al manejo expectante; sin embargo, hasta el 37.5 % de estos puede terminar en choque hemorrágico y la mortalidad puede ser tan alta, como el 25 %, especialmente cuando se asocian a terapia anticoagulante 6.
A continuación, se presenta un caso inusual de HEPA asociado a anticoagulación con rivaroxabán, sin otros factores precipitantes y que fue manejado exitosamente con embolización arterial selectiva.
Presentación del caso
Mujer de 74 años con antecedente de hipertensión arterial, hipotiroidismo, enfermedad trom-boembólica recurrente e hipertensión pulmonar asociada. Tuvo un último evento trombótico tres años previo a su ingreso, por trombosis venosa profunda y embolia pulmonar, por lo que venía anticoagulada con 15 mg al día de rivaroxabán. Adicionalmente, refería nefrectomía derecha en 2011, de etiología no clara.
Consultó por un cuadro de 24 horas de evolución de dolor en el hemiabdomen izquierdo, tipo urente, progresivo, en intensidad hasta alcanzar 10/10 en la escala visual análoga. No refería fiebre ni otros síntomas. Negaba algún tipo de trauma. En el examen físico se encontraba álgica, con signos vitales estables, con masa palpable en el flanco izquierdo y marcado dolor a la palpación, sin irritación peritoneal.
En el ingreso, el hemograma, la función renal y los tiempos de coagulación fueron normales, con concentraciones de hemoglobina de 12.4 g/dL. Durante la observación en la sala de reanimación, en las primeras 6 h la paciente tuvo hipotensión de 68/37 mmHg y diaforesis profusa. Ante la sospecha de hematoma con sangrado activo, se revirtió la anticoagulación con plasma fresco congelado y se llevó directamente a angiotomografía de abdomen contrastada, que mostró un hematoma del músculo recto abdominal izquierdo de densidad heterogénea, con áreas hiperdensas de 195 x 70 x 112 mm y se visualizó un pequeño foco lineal hiperdenso en la fase venosa sugestivo de sangrado activo (figura 1).
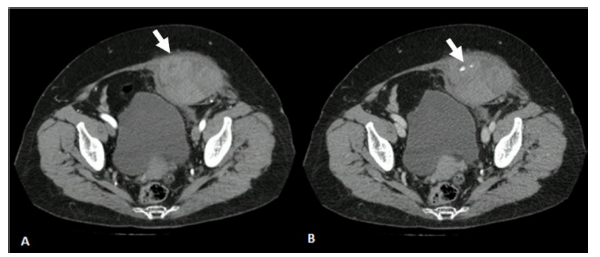
Figura 1
Angiotomografía de abdomen contrastada (corte transversal). A) Fase arterial, hematoma en el músculo recto abdominal izquierdo de densidad heterogénea (195 x 70 x 112 mm [L x AP x T]) (flecha). B) Fase venosa, foco lineal hiperdenso correspondiente a sangrado activo (flecha)
Dada la inestabilidad hemodinámica y el sangrado activo, se llevó a aortograma y arte-riografía de vasos abdominales 14 h después de su ingreso. El servicio de radiología intervencionista realizó el procedimiento, identificando un punto compatible con extravasado de contraste en el territorio de la arteria epigástrica inferior izquierda. Esta se embolizó con material temporal reabsorbible (Spongostán®) y se obtuvo la oclusión completa.
Posterior al procedimiento, la paciente fue trasladada a la unidad de cuidados intermedios. Se logró su estabilidad hemodinámica y se documentó anemización con una hemoglobina de 9.2 g/dL; sin embargo, no requirió transfusión, y en los días siguientes hubo estabilidad, con la hemoglobina en 10.8 g/dL, al tercer de día de su ingreso.
Posteriormente, fue trasladada a una sala general, donde, dada la estabilidad clínica y de acuerdo con el concepto de clínica de anticoagulación, se definió reiniciar la anticoagulación 5 días luego de la embolización. Al evaluar los eventos tromboembólicos venosos de la paciente, se documentó tromboembolismo pulmonar crónico, por lo que se consideró el anticoagulante de elección, en este caso warfarina.
Ante la presencia de dolor abdominal, a la paciente se le realizó una ecografía de control, que mostró hematoma residual en fase crónica, sin signos de sangrado activo. Egresó 9 días después de su ingreso, con el International Normalized Ratio (INR) en 2.4, en rango terapéutico y con seguimiento con clínica de anticoagulación. Al mes siguiente, en consulta externa se valoró a la paciente, quien para el momento tenía resolución total del hematoma, sin eventos de nuevos sangrados y con el INR en 2.13, por lo que continuó seguimiento por clínica de anticoagulación.
Discusión
El HEPA es una entidad poco frecuente. La mayoría se debe a sangrado de la aponeurosis del músculo, típicamente secundario a trauma en las arterias epigástricas o directamente sobre el músculo 8. Las formas espontáneas son menos frecuentes y se han visto asociadas principalmente con el uso de anticoagulantes orales, como la warfarina (69 %); pero también con anticoagulantes de uso parenteral 5,7. Otros factores asociados son el embarazo, la hipertensión arterial, el antecedente de cirugía abdominal reciente, los defectos de coagulación y la terapia antiagregante 7,9. Se describen también factores desencadenantes, como los accesos de tos, pujo y vómito 5,7,8. En el caso presentado no se encontraron otros factores de riesgo o desencadenantes diferentes a la anticoagulación terapéutica.
El dolor abdominal de inicio súbito y la aparición de masa abdominal son la presentación clínica más frecuente 5,8,10, al igual que en este caso. El diagnóstico se basa en el abordaje clínico e imágenes como la tomografia computarizada de abdomen, descrita como el estudio con mayor sensibilidad 11. Aunque la anticoagulación es el principal factor de riesgo, son pocos los reportes de HEPA en pacientes con uso de ACOD. Algunos casos se han descrito con apixabán y rivaroxabán; sin embargo, a diferencia de la paciente de este caso, la tos fue un posible desencadenante, y en todos se dio manejo quirúrgico 12-14. Adicionalmente, en una serie de casos de 2020 con 99 pacientes los autores informaron que el 5.7 % se encontraba en manejo con ACOD, pero no hubo claridad acerca de factores desencadenantes diferentes a la anticoagulación y ninguno requirió manejo invasivo 9. Por el bajo número de casos documentados con este tipo de anticoagulantes, no es claro si existe una diferencia en su presentación con los otros anticoagulantes o si se relaciona con el nivel de anticoagulación.
La mayoría de los casos son autolimitados y se reporta un 4 % de mortalidad; sin embargo, esta aumenta hasta un 25 % en pacientes anticoagulados 15. Otros factores asociados con mayor mortalidad son la enfermedad renal crónica estadio 3 y la necesidad de transfusión 7. En el caso que se describe, se resaltan factores de riesgo para mayor mortalidad, como lo es enfermedad renal crónica dada por ser monorrena y la asociación con anticoagulación terapéutica. Aquí la ventaja fue un manejo exitoso y temprano de embolización arterial selectiva, al contar en el hospital con un servicio permanente de radiología intervencionista. En otros estudios retrospectivos se ha descrito que la embolización selectiva mejora diferentes desenlaces, como mejor control del sangrado, menos días de estancia hospitalaria e incidencia de choque hipovolémico; sin embargo, el manejo con radiología intervencionista no es el más frecuente en la mayoría de series de casos 9,15.
Un estudio retrospectivo identificó que los factores predictores de falla al tratamiento conservador eran la extravasación activa del medio de contraste en la tomografía, un mayor volumen del hematoma y trasfusión de más de 4 unidades de glóbulos rojos empaquetados. En el presente caso se identificaron dos de estos factores, por lo que lo indicado era un manejo intervencionista temprano. En lo revisado, este es el primer reporte de HEPA exclusivamente asociado a anticoagulación con ACOD y que recibió manejo exitoso con embolización arterial selectiva.
Conclusión
El HEPA es una entidad poco frecuente y potencialmente fatal. La anticoagulación es el principal factor asociado descrito; pero hay pocos casos reportados con el uso de ACOD. En la mayoría de las ocasiones, la suspensión de la anticoagulación y el manejo expectante pueden ser suficientes como tratamiento. No obstante, teniendo en cuenta su alta mortalidad o predictores de falla al manejo conservador, se debe contemplar de forma temprana el manejo endovascular, como una estrategia para el tratamiento exitoso en casos severos que además permitirá un reinicio más temprano de la anticoagulación.